背景:
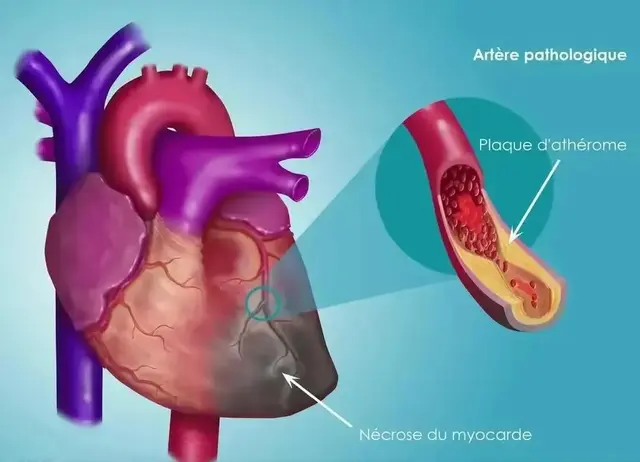
動脈粥樣硬化導致血管變窄,限制血液流動,是心血管疾病的主要原因,占全世界死亡總死亡人數的近三分之一。盡管醫療技術的進步和死亡率的降低,但預計未來死亡總數還會增加,這表明在動脈粥樣硬化的臨床管理方面需要繼續進行技術創新。
基于此,Junbo Ge等人混合生物仿生脂體與血小板膜(P-Lipo)融合,用于動脈粥樣硬化靶向(圖1)。天然血小板膜和人工脂質膜通過擠出法融合,形成混合納米球,有望保持血小板和脂質物理化學和藥物特性的靶向能力。

圖1 仿生納米藥物示意圖
P-Lipo的制備和定性
脂質體是由薄膜水化制備的,P-Lipo是通過用擠出法融合血小板膜囊泡(PMV)和脂質體而制造的,拉帕黴素被添加到脂質中,以構建RAP-P-Lipo。脂質體作爲藥物輸送系統的主要限制之一是儲存過程中的中度穩定性和聚集風險,這導致需要特殊的儲存和遞送條件。實驗結果表明,血小板膜融合增強了空氣中室溫下脂體的穩定性,這可能是由于天然抗氧化作用和天然膜上存在的大量表面糖,可能降低儲存條件的要求。

圖2 P-Lipo的表征
P-Lipo定位和滲透作用
P-Lipo的結合和滲透能力通過體外培養脂質體與人頸動脈斑塊來評估。人動脈粥樣硬化斑塊的組織學分析顯示,P-Lipo(紅色)在斑塊組織中廣泛積累和更深滲透,而斑塊組織中幾乎沒有Lipo積累,大部分Lipo僅限于斑塊邊界。這些結果表明,血小板膜裝飾可有效增強P-Lipo的斑塊分布和滲透。此外,P-Lipo還顯示出優于PNP的斑塊滲透能力。

圖3 定位和滲透作用
P-Lipo定位和生物分布
爲了評估P-Lipo在體內動脈粥樣硬化的靶向能力,將脂質體靜脈注射到ApoE−/−以西式飲食餵養8周的老鼠。與注射P-Lipo的小鼠的正常主動脈相比,P-Lipo優先積聚在動脈粥樣硬化斑塊處並産生更高的熒光強度,表明P-Lipo特異性靶向動脈粥樣硬化斑塊。單獨的抗體對主動脈瓣切片進行染色,包括IV型膠原蛋白、激活內皮細胞的vWF以及巨噬細胞的CD68。結果顯示,切片上P-Lipo信號的高度接近或共定位(圖4)。這些結果表明,具有天然血小板膜融合的P-Lipo優先分布並滲透到具有多因素生物結合的動脈粥樣硬化斑塊中。

圖4 P-Lipo的定位和生物分布
RAP-P-Lipo抗動脈粥硬化
爲了證實P-Lipo制劑在抗動脈粥樣硬化治療中的效用,P-Lipo加入了具有強大動脈粥樣硬化保護作用的RAP。負載RAP的脂質體納米顆粒與其他納米顆粒相比,顯示出優異的抗動脈粥樣硬化作用。實驗結果表明,RAP-P-Lipo表現出最強的抗動脈粥樣硬化功效。顯示最小斑塊面積和更穩定的斑塊,顯著減少了主動脈根部的斑塊病變和斑塊中巨噬細胞陽性面積。這些結果表明,P-Lipo靶向遞送RAP通過減弱動脈粥樣硬化的發展和穩定動脈粥樣硬化斑塊,顯著增強了RAP的抗動脈粥樣硬化作用。

圖5 RAP-P-Lipo抗動脈粥樣硬化功效
P-Lipo安全性和免疫原性
Q-Lipo的全身給藥並未引發小鼠的炎症反應。P-Lipo組和Lipo組血清細胞因子(TNFα、IL-1β和IL-6)水平無顯著差異。H&E染色顯示在主要器官中沒有觀察到明顯的組織病理學異常或損傷。此外,IgM和IgG陽性P-Lipo和Lipo的流式細胞術譜沒有顯示出可觀察到的自體抗體滴度升高。這些結果表明,作爲靶向遞送平台,P-Lipo沒有啓動顯著的適應性免疫反應,對治療的小鼠沒有顯著的負面影響,表明P-Lipo治療動脈粥樣硬化的毒性或風險低。

圖6 P-Lipo的安全性和免疫原性
相關成果近期在國際著名期刊Chemical Engineering Journal(2020年影響因子13.273)以題爲Biomimetic liposomes hybrid with platelet membranes for targeted therapy of atherosclerosis的論文發表。
論文相關鏈接:
https://www.sciencedirect.com/science/article/pii/S1385894720334203