5月9日,正大天晴藥業集團申報的1類創新藥貝莫蘇拜單抗注射液Benmelstobart (TQB2450)(商品名“安得衛”)首個適應症國家藥品監督管理局(NMPA)批准上市,聯合鹽酸安羅替尼膠囊、卡鉑和依托泊苷用于廣泛期小細胞肺癌(ES-SCLC)患者的一線治療。

截圖來源于國家藥品監督管理局
此次獲批是基于一項隨機、雙盲、安慰劑對照、多中心III期臨床試驗(ETER701),該研究結果于2023年世界肺癌大會(WCLC)上公布:
主要終點結果顯示,貝莫蘇拜單抗+安羅替尼+EC組vs安慰劑+EC組的中位總生存期(mOS)分別爲19.3個月 vs 11.9個月,mOS顯著提升7.4個月,刷新了ES-SCLC一線治療的現有生存數據。24個月OS率幾乎翻倍,分別爲41.83% vs 24.24%。

截圖來源于“參考文獻1”
兩組的無進展生存期(mPFS)分別爲6.9個月 vs 4.2個月,mPFS顯著延長2.7個月,疾病進展風險降低68%。12個月PFS分別爲27.9% vs 2.3%。
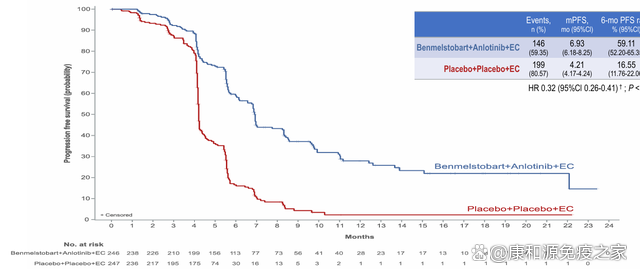
截圖來源于“參考文獻1”
次要終點結果顯示,貝莫蘇拜單抗+安羅替尼+EC組vs安慰劑+EC組的中位緩解持續時間(mDoR)分別爲5.8個月vs3.1個月,總緩解率(ORR)分別爲81.3%vs 66.8%。疾病控制率(DCR)分別爲90.7% vs 87.0%。
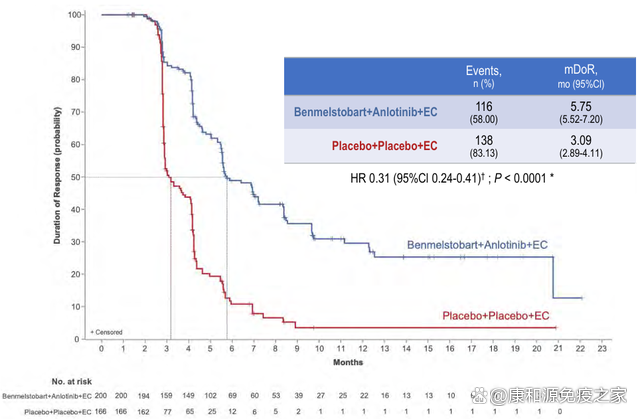
截圖來源于“參考文獻1”
中國臨床腫瘤學會發布的《小細胞肺癌診療指南2023》顯示,小細胞肺癌占肺癌的13%—17%。根據國家癌症中心發布的癌症調查數據,2022年新發現小細胞肺癌人數約爲16萬人。小細胞肺癌分爲局限期和廣泛期,約70%的患者初診時已爲廣泛期。此次貝莫蘇拜單抗適應症的獲批,爲小細胞肺癌帶來新的治療選擇。
貝莫蘇拜單抗是正大天晴自主研發的一款全新序列的創新人源化抗PD-L1單克隆抗體,可阻止PD-L1與T細胞表面的PD-1和B7.1受體結合,使T細胞恢複活性,從而增強免疫應答,被認爲具有多種腫瘤的治療潛力。
除了晚期小細胞肺癌,貝莫蘇拜單抗與安羅替尼聯用治療複發性或轉移性子宮內膜癌的適應症也已于今年2月申報上市,並被CDE(國家藥監局藥品審評中心)納入優先審評審批程序。早在2022年4月,該療法已被CDE列爲突破性品種。
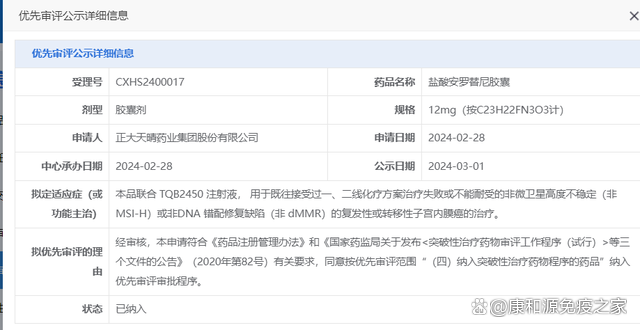
截圖來源于“國家藥品監督管理局藥品審評中心”
綜上所述,貝莫蘇拜單抗聯合安羅替尼及化療的四藥方案在一線廣泛期小細胞肺癌適應症取得了優異的臨床數據,將給患者帶來全新的治療選擇。
參考文獻
1.WCLC23S4Benmelstobart.pdf(oncoletter.ch)
2.OA01.03 Benmelstobart with Anlotinib plus Chemotherapy as First-line Therapy for ES-SCLC: A Randomized, Double-blind, Phase III Trial - Journal of Thoracic Oncology (jto.org)
免責聲明:康和源免疫之家爲腫瘤科普平台,文本參考來源于網絡,版權歸原作者所有。
該文章僅供分享,如涉嫌侵犯您的著作權請聯系我們刪除,謝謝!
