研究背景
生物-機器接口和生物醫學工程技術的出現,如表皮電極、多模式生理信號監測、生物傳感、神經元電記錄和刺激、感覺運動功能修複、虛擬現實和增強現實等,均迫切需要一種具有高效觸覺傳感能力和生物相容性的堆疊傳感平台,以檢測人類皮膚的生理功能,並使工業機器人和假肢技術能夠感知觸覺信息。水凝膠,以其獨特的類固體粘彈性、類液體滲透性和溶脹特性,以及模擬體內微環境的能力,成爲觸覺傳感領域極具前景的基質替代品。然而,最先進的基于聚合物水凝膠的觸覺傳感器和電子皮膚技術存在不可逆的共價結合、難以調控的物理化學性質和有限的生物相容性,從而限制了其在生物-機器界面領域的廣泛應用。肽超分子水凝膠,即由各向異性自組裝糾纏的3D納米纖維網絡,在各種生物醫學和生物機器界面應用中補充聚合物對應物,引起了越來越多的興趣。其中,Fmoc-FF水凝膠憑借其超快的自組裝動力學、細胞外基質狀3D網絡、模擬生物受限系統的粘性水納米池以及出色的共組裝特性,展現出作爲開發觸覺傳感平台的生物啓發超分子基質的潛力。然而,機械剛度較弱和自組裝過程的調控難度較大,嚴重阻礙了Fmoc-FF水凝膠在觸覺傳感應用中的進一步發展。
研究成果
近日,浙江大學陶凱研究員、潘定一教授和修鵬副教授,通過引入聚乙二醇二丙烯酸酯(PEGDA)來調控9-芴甲氧羰基-改性二苯基丙氨酸(Fmoc-FF)的自組裝,成功實現了從較薄的納米纖維到更寬納米帶的轉變,將超分子水凝膠的機械性能提高了10倍,爲觸覺傳感提供了生物啓發的超分子封裝基底。此外,通過摻雜PEDOT:PSS和9-芴甲氧基羰基改性的3,4-二羟基-L-苯丙氨酸(Fmoc-DOPA),將Fmoc-FF自組裝水凝膠設計成具有導電性和粘性的材料,爲觸覺傳感應用提供仿生傳感單元和粘合層。因此,這些模塊的集成産生了基于肽水凝膠的觸覺傳感器,顯示出高靈敏度和可持續的響應,同時具備出色的生物相容性和生物降解性。這一發現爲觸覺傳感應用開發具有可調節特征的可編程肽自組裝奠定了可行性。相關研究工作以“Bioinspired Flexible Hydrogelation with Programmable Properties for Tactile Sensing”爲題發表在國際頂級期刊《Advanced Materials》上。

研究內容
通過引入PEGDA作爲共溶劑,成功使Fmoc-FF自組裝體系的結構從傳統的較薄納米纖維轉變爲納米螺旋,然後再到納米帶,從而使水凝膠的楊氏模量提高10倍,這表明其是用于觸覺傳感的受生物啓發的包封基底。接下來,通過Fmoc-FF與PEDOT:PSS和Fmoc-DOPA的共組裝,將自組裝的納米纖維水凝膠進一步設計成導電和粘合的,從而爲觸覺傳感器提供仿生傳感單元和粘合層。因此,模塊的集成可以産生基于Fmoc-FF水凝膠的觸覺傳感器,具有內在生物相容性和生物降解性,且表現出與最先進聚合物對應物相當的性能,如靈敏度和耐用性(方案1)。研究成果證明了基于肽的可編程超分子水凝膠用于觸覺傳感的可行性,從而爲生物-機器界面和生物醫學工程應用提供了生物啓發的替代品。

方案1. 基于觸覺傳感器的仿生超分子水凝膠的發展示意圖
1、Fmoc-FF自組裝的形態調控
爲了深入研究PEGDA700對Fmoc-FF水凝膠自組裝的影響及其力學特性,進行了TEM表征。具體而言,當χPEGDA700爲零時(原始Fmoc-FF水凝膠),觀察到直徑爲12.7±1.9nm的薄且密集的納米纖維(圖1a(i))。隨著χPEGDA700增加到5%(v.),納米纖維的直徑增加至17.2±3.7nm,且捆綁趨勢減弱(圖1a(ii))。當χPEGDA700增加到10%(v.)時,TEM圖像主要顯示廣泛分布、不均勻、寬的納米帶,同時納米纖維數量減少且直徑爲26.4±6.5nm(圖1A(iii)),證實了薄納米纖維逐漸轉變爲寬納米帶。事實上,當χPEGDA700設定爲7.5%(v.)時,大量直徑爲40.2±8.9nm的左旋納米螺旋結構(圖1b)主導了TEM圖像,這些納米螺旋的尺寸大于納米纖維,並展示了階梯狀紋理(圖1b插圖),從而揭示了Fmoc-FF自組裝經曆的分級過程,納米螺旋是納米纖維和納米帶之間的過渡階段,這在以前的報告中鮮有實驗驗證。
當χPEGDA700進一步增加至15%(v.)時,寬度爲245.4±70.7nm的均勻納米帶占據了主導地位(圖1A(iv)),揭示了PEGDA700的強溶解能力能夠完全消除Fmoc-FF自組裝過程中的扭曲現象。隨後,隨著χPEGDA700增加到20%(v.),細長的自組裝體不再存在,並且觀察到寬度爲27.5±7.0nm的聚集片段(圖1A(v)),表明Fmoc-FF單體在高比例的PEGDA70下不能組織成更大的結構。可以得出結論,PEGDA700的引入,使Fmoc-FF自組裝經曆了從薄納米纖維到寬納米帶的轉變,其中納米螺旋作爲中間體(圖1C)。

圖1. 依賴Fmoc-FF自組裝的PEGDA700
2、Fmoc-FF水凝膠的機械增強
結構演變會影響生物啓發的超分子水凝膠的力學特性。具體而言,在增加χPEGDA700時,系統的儲能模量(G')呈現抛物線演變趨勢。與原始Fmoc-FF水凝膠的40.5±10.9kPa相比,當χPEGDA700達到15%(v.)時,G'顯著提升至438.1±53.6kPa(圖2a),從而證明較寬納米帶的交聯比較薄納米纖維的交聯更有效。然而,隨著χPEGDA700的進一步增加,由于自組裝體的碎片化,G'又出現了明顯的下降(圖2a)。
爲了闡明結構解扭曲誘導的機械性能增強的機制,創建了納米纖維和納米帶的數值模型,並通過介觀耗散粒子動力學方法進行了流體動力學模擬(圖2b)。模擬結果表明,當施加振蕩剪切時,與基于納米纖維的水凝膠相比,基于納米帶的水凝膠顯示出更大的複雜響應函數實部(圖2c),對應于實驗中更高的G'。在這兩個系統的應變-應力曲線(利薩如曲線)中也觀察到了類似的結果(圖2d),基于納米帶的水凝膠在相位差上表現得更爲顯著。模擬和實驗的協同作用表明,Fmoc-FF自組裝剛性、基于納米帶和柔軟的納米纖維水凝膠可以分別用作封裝基底和傳感單元,以開發適用于可穿戴和植入式應用的仿生觸覺傳感器。
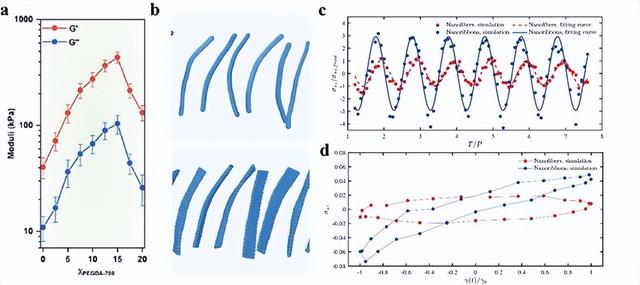
圖2. Fmoc-FF水凝膠的PEGDA700相關機械性能
3、基于Fmoc-FF水凝膠的觸覺傳感器
爲了促進仿生水凝膠的觸覺傳感應用,引入了聚(3,4-亞乙基二氧噻吩):聚(苯乙烯磺酸鹽)(PEDOT:PSS)與Fmoc-FF共組裝,以開發壓阻傳感單元。具體而言,當PEDOT:PSS的質量分數(ω)增加到0.2%(wt.)時,系統G'從原始的42.8±4.6kPa略微降低至33.3±3.3kPa(圖3a藍線),其中二肽單體自組裝成離散的、碎片化的納米纖維,而非之前研究的成束、較長的納米纖維(圖3b上)。同時,系統的電導率從最初的8.9±2.8μS·cm-1提高到396.4±26.5μS·cm-1(圖3a紅線)。然而,當ωPEDOT:PSS進一步增加到0.4%(wt.)時,納米棒成爲主導形態(圖3b下),導致超分子水凝膠的彈性急劇下降,G'僅爲12.9±2.1kPa(圖3a藍線),系統失去自保持能力。因此,考慮到機械性能和導電性能之間的權衡,選擇含有ωPEDOT:PSS=0.2%(wt.)的Fmoc-FF共組裝納米纖維水凝膠來開發用于觸覺傳感的傳感單元。
爲了開發一種實用的高靈敏度觸覺傳感器,設計了一個空間分辨率爲6mm、厚度爲3mm的3×3網格傳感陣列,以高效地檢測負載壓力。隨後,將具有最高儲能模量值的χPEGDA700=15%(v.)的Fmoc-FF自組裝納米帶基水凝膠模作爲包封層。采用ωPEDOT:PSS=0.2%(wt.)的納米纖維水凝膠作爲敏感複合材料,由兩個柔性印刷電路包圍,形成壓阻傳感單元(圖3c)。由于彈性低于封裝層,一旦受到靜態載荷,傳感單元産生的應變比周圍基板更高,這在傳感器陣列的縱向截面應變分布中得到了證實(圖3c插圖)。
基于Fmoc-FF水凝膠的觸覺傳感器的∆R/R0演化曲線,在壓力低于和高于8.0kPa時分別表現出S1=5.7%kPa-1和S2=0.5%kPa-1的兩個分段斜率(圖3d),檢測極限範圍爲0.4kPa-15.0kPa,表明其靈敏度優于先前報道的由聚合物水凝膠組成的觸覺傳感器,如藻酸鹽(SA)/二氧化硅納米纖維(4.1%kPa-1)、聚乙烯醇(PVA)/SA(3.3%kPa-1)和PVA/聚丙烯酰胺(PAAm)(~5.0%kPa-1),從而展示了其在觸覺傳感領域中的巨大潛力。

圖3. 基于Fmoc-FF水凝膠的觸覺傳感器的開發和表征
4、用于觸覺傳感應用的可編程Fmoc-FF水凝膠
肽的生物啓發性質賦予了它們在生物醫學和生物機器接口應用中的可行性。本工作首次研究了Fmoc-FF水凝膠的生物相容性和生物可降解性。具體而言,通過在小鼠體內皮下植入,評估了Fmoc-FF自組裝納米帶基水凝膠在χPEGDA700=15%(v.)和摻雜Fmoc-FFF納米纖維水凝膠在ωPEDOT:PSS=0.2%(wt)下的體內生物相容性。通過與廣泛使用的明膠交聯水凝膠對照,觀察到在植入7天後,基于Fmoc-FF的水凝膠僅引起輕微的免疫反應,表現爲松散的纖維化包封、低膠原密度,且未見巨噬細胞或異物巨細胞浸潤(圖4a上)。淋巴細胞數量的統計(200μm×200μm視野內)表明,基于Fmoc-FF納米帶的水凝膠的免疫反應性與基于明膠的水凝膠相當(圖4b)。
在引入PEDOT:PSS後,混合水凝膠的生物相容性隨著淋巴細胞數量的增加而略有惡化(圖4a,b),這可能是由于導電聚合物的生物相容性限制。值得注意的是,植入7天後,Fmoc-FF基水凝膠幾乎完全消失(圖4a),可能被酶降解爲氨基酸,這一點通過熒光標記檢測得到了證實。作爲對照,即使在3個月後,明膠基水凝膠仍存在于植入區域。這些發現表明,Fmoc-FF水凝膠具有優異的生物相容性和快速的生物降解性,從而證明了基于肽水凝膠的觸覺傳感器在生物醫學和生物機器界面應用中的可行性。除了其與皮膚成分的內在同源性外,基于Fmoc-FF水凝膠的觸覺傳感器可以用作機器人假肢的仿生電子皮膚。
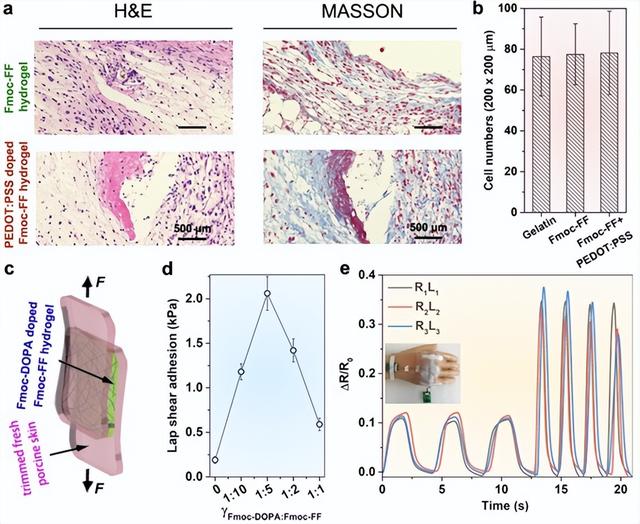
圖4. 基于Fmoc-FF水凝膠的E-皮膚的開發和應用
結論與展望
盡管聚合物基底在觸覺傳感領域應用廣泛,但其有限的生物降解性和生物相容性嚴重制約了其在生物-機器界面和生物醫學工程領域的進一步應用。相比之下,短肽自組裝水凝膠憑借其出色的生物相容性和生物降解性,以及高靈敏度,展現出作爲觸覺傳感器超分子基質的巨大潛力。結合實驗與計算特征,研究者證實Fmoc-FF水凝膠可以靈活編程,以滿足觸覺傳感應用的要求。具體而言,通過引入PEGDA700,有效調控了Fmoc-FF自組裝的形態,從薄納米纖維轉變爲螺旋結構(χPEGDA700=7.5%(v.)),然後進一步演變爲寬納米帶(χPEGDA700=15%(v.))。這顯著提升了生物啓發水凝膠的機械性能,使其成爲先進的聚合物基底的理想替代品,可用于開發觸覺傳感器的封裝層。此外,通過共組裝策略,將Fmoc-FF水凝膠與PEDOT:PSS和Fmoc-DOPA進行摻雜,使Fmoc-FF水凝膠具有導電性和粘附性。尤其,通過優化摻雜比例(ωPEDOT:PSS=0.2%(wt.)和γFmoc-DOPA:Fmoc-FF=1:5),可以最大限度提高導電性和粘附性,爲使用超分子水凝膠設計傳感單元和粘附層提供了切實可行的方案。因此,結合這些組件,開發出了一種基于Fmoc-FF水凝膠的仿生觸覺傳感器,實現對具有固有生物相容性和生物降解性的假體運動的實時監測。
盡管自組裝短肽在觸覺傳感領域尚處于起步階段,但它具有高度的工程性和可編程性。通過調整氨基酸序列、自組裝條件(不同溶劑或氣相沉積)和組織方法(共組裝、共價結合等),可以精確調控生物啓發水凝膠的結構和性質,從而爲開發用于生物機接口和生物醫學應用的合適觸覺傳感平台提供了更多的可能性。肽自組裝顯示出對假肢設備、機器人、可穿戴和植入式設備等提供仿生控制的潛力,爲用戶帶來更自然、高效的交互體驗,有望爲實現具有靈活調節和觸覺傳感能力以及生物相容性的集成檢測平台鋪平道路。
文獻鏈接:
https://doi.org/10.1002/adma.202401678




