阿爾茨海默病是一種神經退行性疾病,影響著全世界5000萬人。據估計,到2050年這一數字將達到1.52億。阿爾茨海默病是導致成年人死亡的第六大原因,主要原因是記憶和認知功能下降。據全球估計,阿爾茨海默病和其它形式癡呆每年花費約6050億美元,相當于全球國內生産總值的1%。據《2023年世界阿爾茨海默病報告》(World Alzheimer Report 2023)預測,到2030年,與阿爾茨海默病和癡呆症相關的費用將從每年1.3萬億美元增加一倍以上,達到每年2.8萬億美元。阿爾茨海默病沒有有效的治療方法,隨著病情的進展,症狀會逐漸惡化。阿爾茨海默病已被世界衛生組織確認爲全球公共衛生重點。
阿爾茨海默病的病理學
與典型的衰老過程不同,阿爾茨海默病是一種進行性神經退行性疾病,表現爲一系列認知障礙,影響日常生活的各個方面。這些損傷影響記憶、思維、決策、溝通、解決問題、個性和行動能力。
阿爾茨海默病的神經病理學特征是神經細胞外β-澱粉樣蛋白聚集形成的斑塊和神經細胞內Tau蛋白過度磷酸化形成的神經原纖維纏結。β-澱粉樣蛋白斑塊和過度磷酸化的Tau蛋白神經纖維纏結的形成導致炎症和認知功能逐漸下降。β-澱粉樣蛋白斑塊最初在大腦的基底、颞區和眶額新皮質區發生,最終擴散到新大腦皮質、海馬、杏仁核、間腦和基底神經節。目前已經提出了一些假說來解釋β-澱粉樣蛋白肽和神經原纖維纏結在阿爾茨海默病神經退行性病變中的作用機制,包括澱粉樣蛋白級聯假說、Tau蛋白過度磷酸化假說和氧化應激假說。此外,氧化應激、線粒體功能障礙和神經炎症在大腦神經病理改變中起著至關重要的作用。
β-澱粉樣蛋白肽β-澱粉樣蛋白(Aβ)是一種跨膜蛋白,通過澱粉樣蛋白生成途徑水解澱粉樣前體蛋白産生。該過程由β-位澱粉樣前體蛋白裂解酶1所啓動,形成一個大的可溶性蛋白和一個99個氨基酸的C端片段(C99)。C99片段經γ分泌酶進一步加工産生40或42個氨基酸形式的β-澱粉樣蛋白。Aβ42水平在阿爾茨海默病發病的早期事件中起著重要作用,尤其是Aβ42/Aβ40的比值。此外,Aβ單體聚集成低聚物、原纖維和澱粉樣蛋白原纖維。澱粉樣蛋白原纖維較大且不溶,它們可以形成斑塊,而澱粉樣蛋白的低聚物可以在整個大腦中移動。
Tau蛋白神經原纖維纏結由成對的螺旋絲和直絲組成,其中含有微管相關蛋白tau的異常磷酸化形式。Tau蛋白主要存在于大腦的神經元軸突中。當tau蛋白被乙酰化或截斷時,它就無法與微管結合,從而促進tau蛋白聚集、線粒體功能障礙和突觸缺陷。
氧化應激氧化應激在阿爾茨海默病病理發生和發展中起著重要的作用。當活性氧和活性氮等自由基增加時,就會發生氧化應激。在應激條件下,線粒體內活性氧的形成增加,從而增加患阿爾茨海默病的風險。在阿爾茨海默病中,氧化應激促進β-澱粉樣蛋白沉積和tau蛋白過度磷酸化以及隨後的突觸和神經元丟失。

微生物-腸-腦軸
腸腦軸是腸道神經系統和中樞神經系統之間的雙向交流系統,建立了大腦的情緒和認知功能與外周腸道功能之間的聯系,而腸道菌群在腸腦軸功能中發揮重要作用,影響神經系統、免疫系統和內分泌系統。腸道菌群産生多種神經活性物質,比如神經遞質、短鏈脂肪酸等細菌代謝物,它們影響神經活動和大腦功能。這些物質是由腸道細菌發酵膳食纖維和其它成分(比如一氧化氮、氨和乙醇)所産生的。
最近的證據表明,微生物-腸-腦軸可以爲抑郁症和阿爾茨海默病等神經退行性疾病的早期診斷和治療提供獨特見解。腸道菌群在阿爾茨海默病發病機制中的作用已被廣泛探索,阿爾茨海默病和輕度認知障礙患者的腸道菌群多樣性指數都要低于健康對照者。此外,研究表明輕度認知障礙和阿爾茨海默病患者的腸道菌群具有相似性,這爲癡呆前期發病機制和高危個體的識別提供了潛在的見解。最近的研究表明,腸道菌群失調與β-澱粉樣蛋白的聚集、tau蛋白的發育、神經炎症和氧化應激的發生之間的聯系與阿爾茨海默病有關。
許多研究都在追求了解和減輕阿爾茨海默病病理的可變風險因素,比如生活方式、不同類型的飲食模式和肥胖。這些外部因素在阿爾茨海默病的發生中起著至關重要的作用。相反,研究表明,健康飲食可能提供一種非藥物治療方法來調節阿爾茨海默病的神經病理標志物。
腸道菌群與阿爾茨海默病的關系
人類腸道菌群包括細菌、真菌、古生菌、病毒和原生動物,它們與人類宿主互惠互利,和諧共生。在人體腸道中,大約有1000種7000株細菌,其中厚壁菌門(比如乳杆菌、梭菌和真杆菌)和擬杆菌門(包括擬杆菌和普雷沃氏菌)是優勢細菌門。由于內源性腸道菌群的結構、數量、分布和生物學特性是不斷波動的,因此,維持健康的腸道菌群至關重要。
腸道菌群失衡與多種疾病有關,包括阿爾茨海默病。腸道菌群失衡與腸道屏障功能的破壞和腸通透性增加密切相關。腸道屏障受損會導致微生物代謝物釋放到血液中。如果血腦屏障也發生滲漏,一些促炎細胞因子可以進入中樞神經系統,通過激活小膠質細胞和星形膠質細胞引發神經炎症。
動物和人類研究都發現,腸道菌群參與阿爾茨海默病的發病機制。具體來說,研究已經確定了某些微生物與阿爾茨海默病相關的腦脊液生物標志物水平之間的關聯。例如,腦脊液生物標志物(包括Aβ42/Aβ40比值、磷酸化tau蛋白(p-tau)和p-tau/Aβ42比值)的水平較低與梭菌科和丹毒絲菌科細菌的存在之間存在關聯。相反,布勞特氏菌屬和擬杆菌屬與較高的腦脊液生物標志物水平相關。
五項橫斷面研究發現,芽孢杆菌門(毛螺菌科、扭鏈瘤胃球菌、人羅斯拜瑞氏菌、Lachnoclostridium菌、馬文布賴恩特氏菌)與血漿和腦脊液中Aβ和tau蛋白水平之間的關聯。相反,研究發現高水平的別樣杆菌屬和內髒臭氣杆菌與腦脊液中澱粉樣蛋白增加和腦脊液中p-tau減少有關。澱粉樣蛋白負荷與乳杆菌豐度呈負相關,嗜黏蛋白阿克曼氏菌與內側颞葉萎縮呈正相關。
來自臨床和臨床前研究的證據表明,嗜黏蛋白阿克曼氏菌在抑郁、焦慮、阿爾茨海默病、帕金森病等神經精神疾病的發生發展中起著重要作用。然而,一些研究人員發現嗜黏蛋白阿克曼氏菌可以顯著降低阿爾茨海默病小鼠模型的認知功能障礙。它還可以提高産生短鏈脂肪酸和神經遞質的腸道微生物的豐度。此外,他們發現嗜黏蛋白阿克曼氏菌可以減少阿爾茨海默病小鼠中Aβ1 - 42的沉積。然而,嗜黏蛋白阿克曼氏菌的潛在作用機制仍存在爭議。
此外,研究還發現,在阿爾茨海默病患者、輕度認知障礙個體和正常對照中,Fusicatenibacter菌、布勞特氏菌和多爾氏菌較高的豐度與較低的簡易智力狀態檢查量表(MMSE)評分之間存在關聯。然而,Hungatella菌、棲糞杆菌等的存在與較高的簡易智力狀態檢查量表(MMSE)評分相關。
動物和人類臨床研究都報道了阿爾茨海默病患者和阿爾茨海默病轉基因動物模型的腸道菌群在門水平上的改變,特別是厚壁菌門、變形菌門和擬杆菌門。雖然放線菌門和疣微菌門發生了變化,但這些細菌門在阿爾茨海默病患者的腸道中並不常見。與沒有腦澱粉樣變性的人相比,澱粉樣變性患者的腸道菌群組成不同。該研究還發現,與抗炎細胞因子IL-10相比,澱粉樣蛋白陽性患者的促炎細胞因子水平增加,比如IL-6、CXCL2、NLRP3和IL-1β。促炎細胞因子與大腸杆菌/志賀氏菌呈正相關,與真杆菌呈負相關。此外,與年齡和性別匹配的健康對照者相比,阿爾茨海默病患者腸道細菌多樣性減少。另外,與健康對照者相比,阿爾茨海默病患者的厚壁菌門和雙歧杆菌減少,擬杆菌門增加。我國的腸道菌群研究也揭示了阿爾茨海默病患者和健康對照者腸道菌群組成的差異。
盡管這些發現共同表明阿爾茨海默病患者腸道菌群組成發生了變化,但必須注意的是,這些研究主要建立了相關性,關于阿爾茨海默病患者細菌門改變的結果缺乏一致性。
飲食、腸道菌群和阿爾茨海默病
飲食對健康的影響可能是有益的,也可能是有害的。飲食可能在影響腸道菌群方面發揮作用。各種因素,比如飲食模式、菌群特異性幹預和天然補充劑的攝入,都有可能顯著改變腸道菌群的組成。這種改變反過來會影響腸腦軸,可能減輕阿爾茨海默病相關病理學。
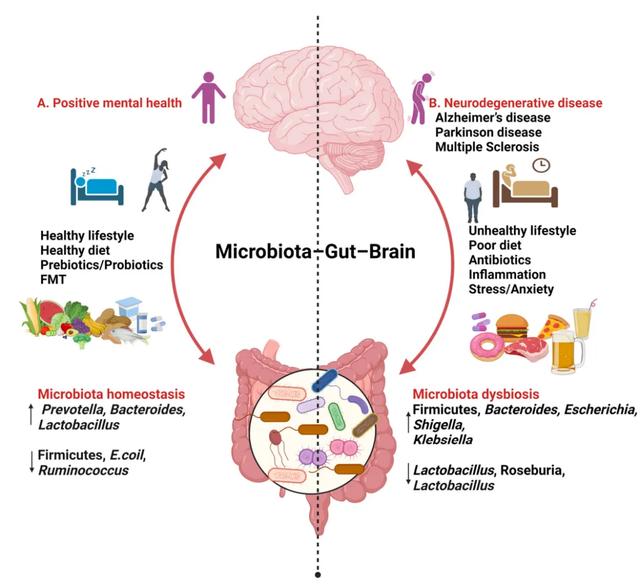
食用脂肪(單不飽和脂肪酸,多不飽和脂肪酸)、碳水化合物(膳食纖維)和蛋白質營養均衡的飲食,同時加入益生菌和益生元,並保持良好的睡眠和運動,與改善心理健康有關。這種飲食模式與有益微生物的增加有關,比如普雷沃氏菌、擬杆菌門和乳杆菌,同時可以降低厚壁菌門、大腸杆菌和瘤胃球菌的水平。
不健康的生活方式、焦慮以及高脂肪、高糖和加工食品的攝入與厚壁菌門、擬杆菌門、埃希氏菌、志賀氏菌和克雷伯氏菌的增加有關,同時與乳酸杆菌、羅斯拜瑞氏菌和擬杆菌門的水平下降有關。
 膳食蛋白質和腸道菌群
膳食蛋白質和腸道菌群蛋白質是人體必需的大量營養素。蛋白質攝入的數量和來源,無論是動物性還是植物性,都會影響整體健康和大腦功能。長期攝入蛋白質可能會影響認知能力下降的風險,蛋白質攝入量越高,主觀認知障礙水平越低。富含蛋白質的飲食與腸道中抗炎細菌(比如青春雙歧杆菌)的減少以及促炎細菌的增加有關。
此外,研究表明,由于産生神經毒性終産物,動物源性蛋白質的攝入與阿爾茨海默病的高患病率之間存在相關性。相反,植物源性蛋白質與降低癡呆症相關的死亡率和改善大腦健康有關。此外,動物蛋白可能通過促進擬杆菌、別樣杆菌和嗜膽菌等厭氧菌的生長而促進炎症。 相反,植物蛋白可以刺激雙歧杆菌和乳杆菌等有益菌的生長,同時減少脆弱擬杆菌和産氣莢膜梭菌等致病菌的生長。
膳食纖維與腸道菌群一般來說,碳水化合物可分爲簡單糖(單糖、雙糖)和複合糖(澱粉、纖維)。膳食纖維是“微生物可利用的碳水化合物”,使微生物能夠爲宿主提供能量。此外,膳食纖維具有改變腸道菌群的能力。因此,膳食纖維被認爲是益生元,簡單糖攝入量的增加與阿爾茨海默病風險的增加有關,而膳食纖維攝入量的增加與阿爾茨海默病風險的降低有關。
可溶性膳食纖維的攝入會促進腸道細菌産生短鏈脂肪酸。有證據表明,在阿爾茨海默病小鼠模型中,攝入可溶性膳食纖維可減少丙酸的形成,增強丁酸的産生,減少星形膠質細胞的激活,並改善認知功能,這些都歸因于腸道菌群的改善。高膳食纖維攝入量的個體表現出有益菌的豐度增加,包括乳酸杆菌和雙歧杆菌,從而降低厚壁菌門/擬杆菌門的比例。
膳食脂肪和腸道菌群膳食脂肪主要有兩種,即飽和脂肪和不飽和脂肪。遊離脂肪酸、單不飽和脂肪和多不飽和脂肪等脂肪的攝入會影響許多有益微生物的功能,比如普雷沃氏菌和雙歧杆菌。單不飽和脂肪和多不飽和脂肪具有積極作用,包括增強腦功能和預防神經退行性疾病。飽和脂肪和反式脂肪的高攝入量與促炎細菌的增加有關,而單不飽和脂肪和多不飽和脂肪的高攝入量可以增加産短鏈脂肪酸的細菌的産生。
研究表明,在小鼠模型中,飽和脂肪會減少抗炎細菌(乳杆菌),增加促炎細菌(梭菌、擬杆菌、嗜膽菌和腸杆菌)。人類相關研究表明,飽和脂肪的攝入會導致放線菌門的增加,而厚壁菌門減少。此外,攝入富含omega-3多不飽和脂肪的魚油可以增加小鼠中有益微生物的豐度,包括雙歧杆菌、乳杆菌、鏈球菌和嗜黏蛋白阿克曼氏菌。在人體研究中,omega-3多不飽和脂肪可以降低厚壁菌門/擬杆菌門的比例,增加産短鏈脂肪酸的細菌的豐度,比如雙歧杆菌、毛螺菌科和羅斯拜瑞氏菌。
膳食多酚多酚是具有抗氧化特性的微量營養素,天然存在于植物和植物性食物中。大多數多酚可以在水果和蔬菜中找到,比如葡萄、黑加侖、可可、黑橄榄和綠橄榄、橙子、蘋果、杏仁、亞麻籽、石榴、紅洋蔥和西紅柿。咖啡、綠茶和葡萄酒中也可能含有多酚。多酚可以影響腸道菌群的組成和多樣性。富含多酚的飲食可以促進有益微生物的生長,比如雙歧杆菌和乳杆菌,並降低病原菌的水平,包括金黃色葡萄球菌、鼠傷寒沙門氏菌和梭菌。除了它們的抗炎特性,多酚及其代謝物還可以防止認知能力下降。研究還發現,膳食多酚可能通過調節微生物-腸-腦軸來預防神經退行性疾病。
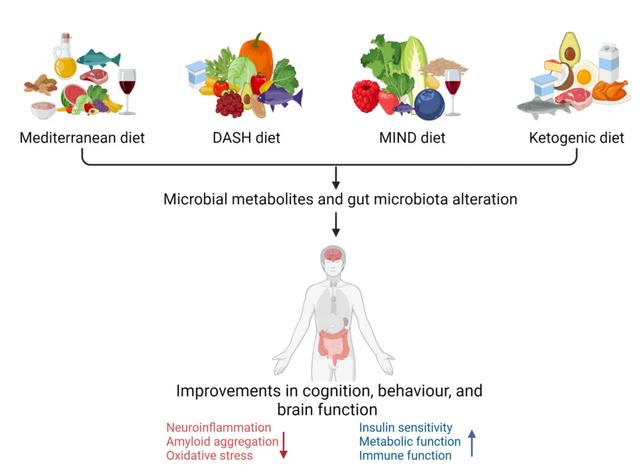 飲食模式和腸道菌群
飲食模式和腸道菌群越來越多的證據表明,富含蔬菜、豆類、谷物、堅果和魚類的飲食以及對植物性食物的偏好,可以改變腸道菌群,這種改變可能預防腸道炎症過程,而腸道炎症過程正是包括阿爾茨海默病在內的許多慢性疾病的基礎。研究最多的飲食模式是地中海式飲食、得舒飲食(DASH)、減緩神經退行性改變的地中海式和DASH飲食(MIND)和生酮飲食。
地中海式飲食、MIND飲食、DASH飲食和生酮飲食之間存在關鍵差異,每種飲食模式所消耗的食物類型不同。所有這些飲食模式都與神經保護特性有關。地中海式飲食與認知能力下降的風險降低有關。DASH飲食也與改善認知功能和降低阿爾茨海默病風險有關。MIND飲食可以降低認知障礙的風險。生酮飲食通過不同的病理生理機制減少或延緩老年人的認知障礙。
一些研究檢查了地中海式飲食,腸道細菌和阿爾茨海默病之間的關系。地中海式飲食包括豐富的蔬菜、水果、堅果、全谷物和橄榄油,適量的魚肉、禽肉和紅酒,以及多酚類物質、膳食纖維和低血糖指數的碳水化合物。因此,地中海式飲食可以促進分解糖的微生物(擬杆菌門、厚壁菌門和放線菌門)的生長以及有益代謝物的釋放。研究表明,攝入地中海式飲食可導致産短鏈脂肪酸的腸道細菌水平升高,比如雙歧杆菌、羅斯拜瑞氏菌和乳杆菌,並降低促炎細菌的水平,比如梭菌。
通過促進有益的纖維降解細菌的生長,地中海式飲食與減少人類全身性炎症有關。根據一項荟萃分析,地中海式飲食依從性也與輕度認知障礙和阿爾茨海默病風險降低有關。這項研究包括34168名參與者,輕度認知障礙風險降低了17%,阿爾茨海默病風險降低了40%。此外,在爲期12個月的時間裏,研究人員對來自5個歐洲國家的612名非體弱或體弱前期個體進行了檢查,研究結果顯示炎症減輕,認知功能得到改善。根據一項對16160名老年人進行的研究,地中海式飲食的追隨者患癡呆的風險降低了20%。堅持10周地中式海飲食對老年人的認知功能也具有有益的影響。
生酮飲食的特點是高脂肪(75%)和高蛋白質(20%)的攝入,碳水化合物的攝入很低(5%),旨在誘導酮症狀態。對輕度認知障礙或阿爾茨海默病患者的研究表明,吃生酮飲食可以顯著改善認知功能,同時改變腸道菌群,影響阿克曼氏菌和副擬杆菌等細菌物種。然而,對人類的研究表明,吃生酮飲食會減少有益微生物,同時增加促炎細菌的水平,比如大腸杆菌和脫硫弧菌。
此外,高度堅持DASH飲食和MIND飲食與降低阿爾茨海默病風險有關。這些飲食模式含有具有抗氧化和抗炎特性的營養素,有助于抑制β-澱粉樣蛋白的沉積。
益生元、益生菌和阿爾茨海默病
益生菌是對宿主健康具有促進作用的活性微生物,而益生元是益生菌的食物,可以選擇性促進腸道有益微生物的生長。使用乳酸杆菌和雙歧杆菌等益生菌來減少神經炎症,越來越受到人們的關注。
益生元和阿爾茨海默病益生元是宿主有益微生物選擇性代謝的底物,從而産生健康益處。最近對動物和人類的研究調查了益生元對心理健康的影響。例如,給阿爾茨海默病小鼠補充益生元甘露聚糖,認知缺陷、澱粉樣蛋白斑塊、氧化應激和小膠質細胞激活減少了,腸道菌群也得到改善。此外,益生元R13原肌球蛋白受體激酶B可抑制腸道中的促炎途徑,導致澱粉樣蛋白生成和氧化應激減少。益生元甘露特鈉(GV-971)被用于增強認知功能和治療輕中度阿爾茨海默病。有證據表明,GV-971可以逆轉認知障礙,糾正腸道菌群失調,抑制神經炎症,並滲透過血腦屏障直接與β-澱粉樣蛋白結合,抑制β-澱粉樣蛋白纖維的形成。
益生菌與阿爾茨海默病益生菌占優勢的腸道菌群可以增強認知功能,並在預防阿爾茨海默病的記憶喪失中發揮積極作用。乳杆菌和雙歧杆菌是最常用的益生菌。補充短雙歧杆菌、長雙歧杆菌和嬰兒雙歧杆菌8周後,腸道菌群組成發生改變,血清和大腦短鏈脂肪酸水平升高。
另一項研究表明,在阿爾茨海默病小鼠模型中,益生菌與維生素制劑結合可降低β-澱粉樣蛋白水平並改善認知能力。同一個研究小組觀察到,補充乳雙歧杆菌Probio-M8 45天時,會導致β-澱粉樣蛋白斑塊數量減少,腸道菌群組成的改變,並改善認知能力。含有嗜酸乳杆菌、幹酪乳杆菌、兩歧雙歧杆菌和發酵乳杆菌的益生菌牛奶可以顯著改善簡易智力狀態檢查量表(MMSE)評分,降低血漿丙二醛和血漿C反應蛋白的水平。輕度認知障礙患者接受短雙歧杆菌A1治療16周,結果發現,與安慰劑組相比,在神經心理評估方面有顯著改善,包括神經心理狀態評估可重複性系列測驗(RBANS)和日本版輕度認知障礙篩查(JMCIS)。
這些研究表明,益生菌、益生元、合成菌(益生菌和益生元的組合)和後生元(益生菌代謝産生的功能性生物活性化合物,比如短鏈脂肪酸)可以有效地改變阿爾茨海默病相關的神經病理和疾病進展,提供了一種新的治療方法。

腸道菌群失調在阿爾茨海默病的病理發生中起著關鍵作用,這爲阿爾茨海默病提供了一種非侵入性診斷和潛在的治療途徑。腸道菌群失調與阿爾茨海默病發病機制之間存在複雜的相互作用,包括β-澱粉樣蛋白和tau蛋白磷酸化異常、神經炎症、神經遞質失調和氧化應激。不健康的飲食和生活方式正是導致腸道菌群失調的最大罪魁禍首,預防老年癡呆,從改變飲食和保護腸道健康開始。
圖片均來自網絡
參考資料:
Dissanayaka, D.M.S.,et al. The Role of Diet and Gut Microbiota in Alzheimer’s Disease. Nutrients 2024,16,412.
