人體胃腸道每天都暴露在潛在的有害物質和成分之中,它們會破壞健康與疾病之間的平衡。胃腸道運輸水和電解質,並向腸腔分泌水和蛋白質。這一動作具有防禦功能,可以阻止有害物質進入腸道屏障。
腸道屏障包含兩層,頂端屏障和基底外側屏障。小腸將食物與來自胰腺、肝髒和腸道的消化液混合,並將它們向前推進,繼續消化過程。小腸細胞壁通過被動擴散、主動運輸和細胞旁轉運等方式吸收營養物質進入血流。兩層屏障的相互作用使腸道內穩態得以維持和平衡,能夠區分共生微生物(對宿主有益)、病原體、營養物質和炎症顆粒。
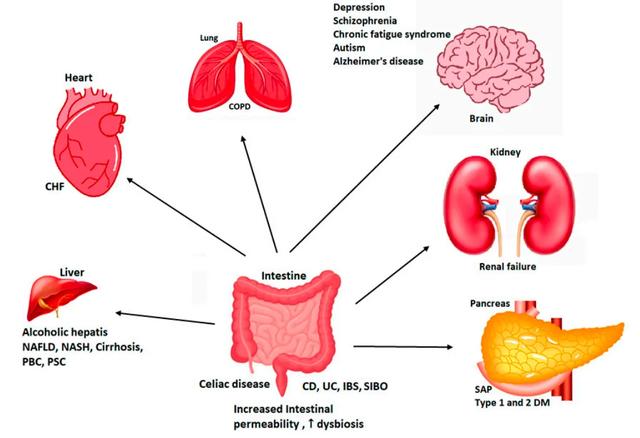
在正常情況下,完整的腸道屏障可以阻止病原體、促炎物質和抗原向內環境的傳播。然而,腸壁完整性的破壞會有利于它們進入,可能引發疾病或炎症。腸上皮屏障功能障礙和通透性增加導致腸漏,它與腸道疾病相關,比如炎症性腸病、腸易激性肝病、酒精性肝病、非酒精性脂肪肝、脂肪性肝炎、肝硬化和乳糜瀉等等。腸漏也與非腸道疾病相關,比如肥胖、糖尿病、癌症甚至包括神經精神疾病等等。
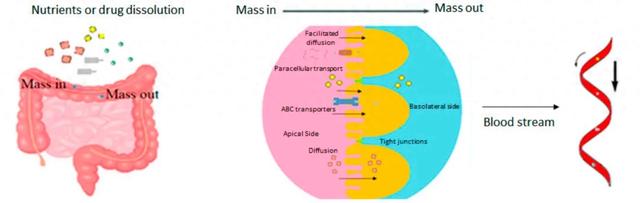
所謂腸道通透性,是指中等大小的親水性分子在不借助載體系統的情況下順著濃度梯度的方向無通過腸上皮的過程。腸道通透性增加是腸屏障紊亂的標志。根據腸漏假說,腸道高通透性可使有害微生物、毒素或未消化的食物顆粒通過腸上皮的連接處進入血液,從而影響激素、免疫、神經、呼吸或生殖系統。事實上,由于緊密連接蛋白功能和/或表達水平的改變而導致的腸道通透性增加會導致腸漏。
采用西方生活方式的國家,炎症性腸病和腸漏的發病率正在上升。其發病機制尚不明確,但與多種因素有關。然而,在遺傳易感的個體中,不同的環境因素會引發免疫反應的改變,因此,對腸道共生微生物的耐受性喪失,導致組織損傷和慢性炎症。
飲食是最重要的環境風險因素之一。高蔗糖、高精制碳水化合物、高多不飽和脂肪酸和omega-6而低膳食纖維的飲食與這些腸道疾病的風險增加有關。由于並非所有患者的反應都是相同的,因此營養建議不能一概適用。營養遺傳學、營養基因組學和表觀遺傳學等學科的出現,使人們對這種疾病的發病機制有了更深入的了解,因此,開啓了從營養角度個性化治療的可能性。治療腸道滲透性的研究主要基于避免大量的糖和脂肪,並實施低FODMAP(可發酵的低聚糖、雙糖、單糖和多元醇)飲食,補充益生元、益生菌、膳食纖維、谷氨酰胺、維生素、短鏈脂肪酸、多酚類物質等等。
腸道屏障的組成部分
腸道屏障從上到下依次是微生物屏障、化學屏障、物理屏障和免疫屏障。化學屏障包含微生物、免疫球蛋白A(IgA)、黏蛋白、單磷酸腺苷(AMPs)和抗菌肽;物理屏障包括腸上皮細胞、杯狀細胞(合成和釋放黏蛋白)、潘氏細胞(合成AMPs)和腸道幹細胞;免疫屏障主要由T細胞、B細胞、巨噬細胞、樹突狀細胞和肥大細胞組成。
第一道防線位于胃腸道和腸腔。腸道屏障是連接機體內外環境的界面。它包括各種有助于免疫功能的物理和化學成分。對病原微生物和抗原的抑制作用是由胃、胰腺和膽汁分泌物作用産生的。消化酶,包括蛋白酶、脂肪酶、澱粉酶和核酸酶,對那些可能來自飲食的病原體發揮屏障作用。健康的腸道菌群能夠與病原體競爭營養物質,代謝蛋白質和碳水化合物,並合成維生素。腸道有益菌群還可以産生許多其它代謝産物,參與調節上皮與免疫系統之間的相互作用,産生抗菌物質,抑制病原體。
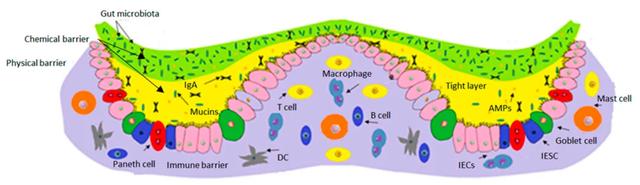
其次,必須從黏液的角度考慮腸道菌群。黏液在整個腸道中各不相同。在小腸中,黏液形成一層薄而不連續的黏液層,這有助于營養物質的吸收;而在大腸中,黏液有兩層。這兩層由沒有細菌的內層和將腸腔與上皮細胞物理分離的外層組成。這些黏液層限制腸道菌群進入上皮的頂端並提供保護。黏液主要成分是水(98%以上)、黏蛋白和糖蛋白。目前已鑒定出超過18種黏蛋白型糖蛋白。來自內層的多糖蛋白複合物(覆蓋在黏膜上皮細胞上的富含碳水化合物的層)和來自外層的MUC2對于疾病預防至關重要。此外,黏液含有分泌型免疫球蛋白A、抗菌産物、三葉肽(三葉因子家族)、抗菌肽cathelicidins和核糖核酸酶,它們負責加強腸道菌群的物理分離,形成從上皮到腸腔的梯度。
第三,腸上皮細胞及其緊密連接是腸道屏障的重要組成部分,將腸道菌群與免疫細胞分離,形成上皮屏障。上皮屏障由一層特化和極化上皮細胞組成的單細胞層,每3-5天更新一次。腸道隱窩中含有多能幹細胞,它們在向絨毛頂端遷移的過程中不斷分裂和分化,産生不同類型的上皮細胞,包括腸細胞、杯狀細胞、腸內分泌細胞和M細胞,它們也可能留在隱窩中,産生潘氏細胞。上皮細胞具有吞噬細菌和中和細菌毒素的能力。上皮細胞還包含模式識別受體和病原體相關分子模式,它們受到嚴格控制,以避免不適當的免疫刺激和炎症。模式識別受體包括Toll樣受體和核苷酸寡聚結構域蛋白。當多肽、抗菌劑、細胞因子和趨化因子的分泌增加時,這些防禦機制會被刺激和激活。
腸上皮下面是固有層,其中含有先天性免疫細胞和適應性免疫細胞,包括巨噬細胞、調節性T細胞、B細胞、中性粒細胞、樹突狀細胞、漿細胞和肥大細胞,以阻止穿透上皮進入的微生物。
腸上皮的細胞間連接
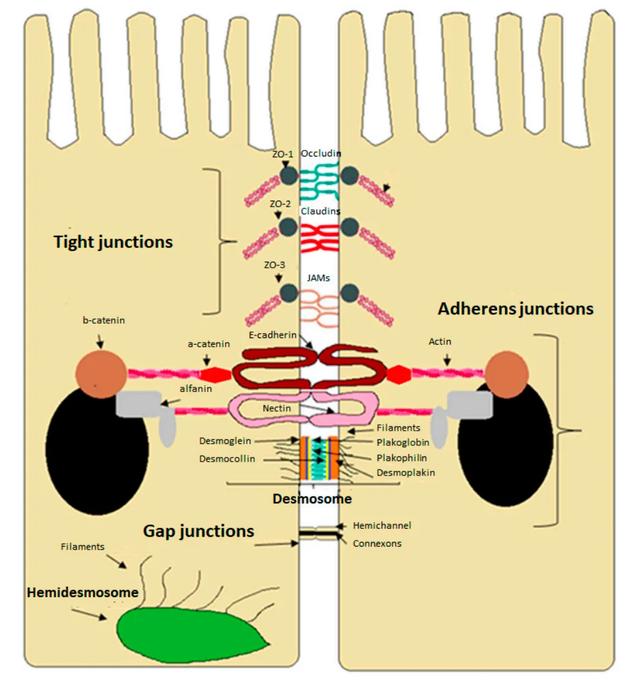
細胞要形成上皮層,需要通過細胞間連接將細胞膜連接到一起。這些連接可分爲三組:細胞間連接、錨定連接和通訊連接。緊密連接蛋白是由位于上皮頂端的多個蛋白在相鄰細胞間聚集而産生的,它控制著細胞旁轉運途徑的通透性,限制離子和溶質的通過。此外,它們通過阻止分子(脂質和蛋白質)從頂端膜到基底外側膜的轉運來維持上皮細胞的極性,反之亦然,因此緊密連接蛋白在腸道屏障的建立中具有非常重要的功能。
緊密連接蛋白受到高度調控,這對于維持正常屏障的完整性至關重要。腸上皮細胞增殖和更新迅速,緊密連接蛋白必須受到調控,以避免對屏障完整性産生任何有害影響。緊密連接蛋白可以適應細胞的不同需求,在不同的生理和病理條件下封閉、打開和維持細胞旁轉運。調控很複雜,由多種蛋白和信號通路完成,比如蛋白激酶C、A和G (PKC、PKA和PKG)、磷酸酶、肌球蛋白輕鏈激酶(MLCK)、絲裂原活化蛋白激酶(MAPK)和磷脂酰肌醇-3激酶通路。閉合蛋白的磷酸化負責打開和關閉緊密連接。緊密連接的可塑性對胃腸道功能、上皮細胞更新和形態發生至關重要。在正常的生理條件下,腸道通透性受到控制,從而維持機體的耐受性和體內平衡。然而,腸道屏障功能的任何缺陷,比如緊密連接以一種不受控制的方式打開,都可能使來自飲食或細菌的抗原通過,這種情況被稱爲“腸漏”。
腸道通透性改變相關疾病
炎症性腸病炎症性腸病最常見的是克羅恩病和潰瘍性結腸炎。兩者的區別主要在于它們影響的腸道區域:前者可出現在整個胃腸道,但主要影響回腸和盲腸;後者主要出現在結腸和直腸。雖然炎症性腸病的病因尚不清楚,但是高水平的腸道炎症與緊密連接的改變有關,有研究發現患者的腸道通透性高于健康人。活動性潰瘍性結腸炎和克羅恩病均與緊密連接蛋白的表達變化有關。基于這些原因,這些疾病患者的屏障功能障礙與炎症反應有關。
腸易激綜合征和其它腸道疾病腸易激綜合征是一種功能性消化系統疾病,表現爲頻繁的腹痛。腸道通透性也與腸易激綜合征的發病機制有關。具體來說,腸易激綜合征患者腸組織中ZO-1蛋白和occludin水平較低。他們研究了外周血單核細胞中細胞因子的産生,這些患者(特別是伴有腹瀉的患者)血清中TNF-α、IL-1β和IL-6的基礎水平升高。
正如我們已經指出的,各種疾病都與腸道菌群失調、微生物易位和腸道屏障功能受損有關,其中包括肥胖、慢性心力衰竭、阿爾茨海默病、癌症、糖尿病和自身免疫性疾病。免疫系統的功能是保護我們免受感染和其它疾病的侵害。然而,在免疫性疾病中,我們的身體成爲侵略者,攻擊身體的細胞,造成損害。
肥胖肥胖是一種慢性疾病,其特征是體內脂肪組織過多。根據世界衛生組織的定義,當BMI等于或大于30時,即爲肥胖。肥胖與腸道通透性增加有關。與野生型小鼠相比,遺傳性肥胖小鼠的腸道通透性、血漿內毒素和促炎細胞因子(比如IL-1β、IL-6、INFγ和TNF-α)增加。另一方面,高脂肪飲食引起的肥胖也與炎症相關的腸道菌群的變化和腸道通透性增加有關。所有這些都表明,肥胖引起的炎症可能與緊密連接的完整性和腸道菌群的改變有關。
非酒精性脂肪性肝炎和非酒精性脂肪性肝病非酒精性脂肪性肝病(NAFLD)是一種由肝細胞內脂肪過度積累引起的肝髒疾病,並且不是主要由飲酒引起。另一方面,非酒精性脂肪性肝炎(NASH)患者,除了脂肪積累外,還可能出現肝髒的其它改變,比如炎症和損傷。NAFLD患者的腸道菌群組成的變化增加了血漿LPS水平,從而引發炎症。這些血漿LPS和促炎細胞因子同時會增加腸道通透性。NAFLD患者腸道通透性增加的主要原因是隱窩ZO-1易位和小腸細菌過度生長。一般來說,NASH和NAFLD與緊密連接完整性受損高度相關。
 慢性心髒病
慢性心髒病 心力衰竭是指心髒不能向身體輸送足夠的血液,因此它不能向身體的其它部位輸送必要的氧氣和營養物質。慢性心力衰竭是最常見的。慢性心力衰竭患者的乳果糖/甘露醇試驗顯示小腸通透性增加35%,三氯蔗糖試驗顯示大腸通透性增加210%。腸道通透性的增加與疾病嚴重程度、靜脈血充血和血清C反應蛋白有關。此外,還發現了高水平的內毒素和炎症細胞因子,比如TNF和STNF-R1。一項對這些患者腸道菌群的研究表明,與健康受試者相比,他們有大量的致病菌,比如彎曲杆菌、沙門氏菌和念珠菌。所有這些都表明,慢性心力衰竭患者腸道屏障功能的改變可誘導細菌易位並觸發細胞因子的産生,從而導致心功能惡化。
乳糜瀉乳糜瀉是一種自身免疫性疾病,具有一定的遺傳成分,由攝入含有麸質的谷物所引起。乳糜瀉患者攝入麸質後,谷物中存在的糖蛋白麥醇溶蛋白穿過上皮到達腸黏膜下層的巨噬細胞,在那裏,促炎分子啓動反應,識別該蛋白爲細胞毒性因子,引起腸道炎症和通透性增加。這種反應會導致緊密連接的結構改變。研究表明,腸道通透性的增加是由于調節緊密連接和細胞旁通透性的連蛋白的增加。雖然麸質可以觸發健康個體和乳糜瀉患者體內連蛋白的釋放,但後者産生的蛋白量要高得多。乳糜瀉會增加腸道通透性,從而誘導細胞骨架重組,破壞緊密連接的完整性。
1型糖尿病糖尿病是一種由身體不能合成胰島素或出現胰島素抵抗而引起的慢性疾病。1型糖尿病是針對宿主胰腺β細胞的自身免疫反應,導致胰島素分泌不足。一些研究表明腸道屏障功能障礙與1型糖尿病之間可能存在關系。首先,對1型糖尿病患者的研究表明,即使在發病之前,腸道屏障功能就已經受損,而且腸道通透性增加。另一方面,最近的研究表明,微生物易位有助于1型糖尿病的發生。綜上所述,這些結果表明腸道通透性在1型糖尿病的進展中發揮重要作用。
影響腸道通透性的因素
腸道菌群失調腸道菌群與免疫系統之間的動態相互作用對于維持腸道內穩態和抑制炎症以及維持腸道屏障完整性至關重要。腸道菌群平衡可以控制致病菌的增殖,刺激免疫系統,産生調節宿主免疫系統並作爲結腸細胞碳源的短鏈脂肪酸以及發酵氨基酸和糖類。腸道菌群的不平衡會改變細胞間緊密連接,使病原體和毒素(細菌脂多糖)得以進入。此外,它誘導黏膜相關淋巴組織的刺激,激活炎症級聯反應、建立慢性炎症過程,從而導致大量組織損傷。
在健康人體腸道中發現的數千種細菌中,90%屬于擬杆菌門、厚壁菌門、放線菌門和變形菌門。變形菌門、埃希氏菌、弧菌、耶爾森菌、螺杆菌和沙門氏菌等致病菌的增加,以及梭菌簇IV和XIVa、擬杆菌、雙歧杆菌或普氏棲糞杆菌等共生菌的減少,可導致腸道菌群失調。腸道菌群組成在整個生命過程中不斷變化,許多因素影響其組成,包括飲食、年齡、基因、藥物攝入、環境、生理和心理壓力等等。
感染感染也會破壞腸道屏障。例如,幽門螺杆菌感染人類的胃,這種細菌會使緊密連接中的ZO-1蛋白重新分配而增加腸道通透性。此外,研究發現,通常不被認爲是哺乳動物病原體的噬菌體,可能對腸漏也有一定影響。這些噬菌體的病理作用表現爲增加腸道通透性以及細菌成分和産物的易位。這種易位被認爲是慢性炎症和腸漏相關的各種多病因疾病的主要誘因之一。然而,由于噬菌體可能與腸漏有關,它可能是由于人類持續暴露于腸道微環境中的噬菌體引起的,噬菌體感染是哺乳動物中一種新的病毒性疾病。盡管如此,還需要進一步的研究來證實噬菌體對腸道菌群的影響,並評估其在不同人類病理中的意義。
抗生素和藥物腸道菌群也會受到抗生素或其它藥物的影響。一項關于不同作用方式的抗生素對人體腸道菌群組成影響的研究表明,抗生素可以增加或減少某些腸道微生物。大環內酯類抗生素是兒童和成人中使用最廣泛的抗生素之一。研究表明,兒童長期服用抗生素會導致腸道菌群的改變,其中放線菌門細菌減少,而擬杆菌門和變形菌門細菌增加。另一方面,克拉黴素是最早用于根除幽門螺旋杆菌的抗生素,在根除幽門螺杆菌後,放線菌門和厚壁菌門數量減少,擬杆菌門和變形菌門數量增加。一些研究表明,萬古黴素會降低糞便菌群的多樣性,表現爲厚壁菌門減少,變形菌門增加。環丙沙星可減少厚壁菌門和放線菌門(特別是雙歧杆菌),增加擬杆菌門的比例,而克林黴素可減少乳杆菌和雙歧杆菌的水平。
此外,其它藥物,比如非甾體消炎藥(NSAIDs)、阿司匹林或撲熱息痛,也會損害胃和腸黏膜,並與胃腸道並發症有關。長期使用這些藥物的患者可能表現爲吸收能力下降,腸道通透性增加。
酒精動物研究表明,酒精可導致腸道通透性增加,這取決于酒精攝入的劑量和時間。酒精也可以通過提取和溶解腸道黏膜脂質,導致腸道黏膜表面疏水性下降,從而導致腸道屏障功能喪失,因爲疏水性是腸道屏障功能的關鍵組成部分。人體研究表明,大量酒精會抑制有益細菌,從而導致菌群失調。飲酒已被證明可改變乙狀結腸活檢中黏膜相關菌群的組成。
壓力在某些情況下,壓力可影響腸道屏障的發育,並且與腸道通透性增加有關。壓力對腸道通透性的影響並不簡單,不僅涉及腸道,還可能涉及大腦。促腎上腺皮質激素釋放因子及其受體在壓力誘導的腸道通透性功能障礙中發揮關鍵作用。在急性壓力反應中,細胞旁通透性與內髒超敏反應有關。早期生活中的壓力也會提高大鼠幼仔的血漿皮質酮水平,它與腸道通透性增加和細菌向肝髒和脾髒的易位有關。人體研究也證實急性壓力可影響腸道通透性。像公開演講這樣的壓力源會隨著皮質醇水平的增加而增加腸道滲透性。
另一種壓力因素,寒冷引起的疼痛,會增加白蛋白的通透性,但這只在女性中發現。在産前,壓力因素也是相關的,因爲壓力大的母親所生的嬰兒的唾液皮質醇水平也較高,變形菌門細菌的相對豐度更高,而乳酸菌(乳杆菌、乳球菌和雙歧杆菌)的相對豐度較低。同樣,嬰兒期腸道菌群組成發生改變,在兒童期會顯示出更高的胃腸道症狀和過敏反應發生率,因此生命早期腸道菌群的異常定殖模式可能在生命後期産生影響。
 飲食
飲食飲食對腸道菌群組成和功能有很大的影響。飲食在腸道菌群構成中發揮主導作用,因爲飲食成分可以顯著改變胃腸道功能,損害腸道屏障的完整性。
碳水化合物和脂類的攝入會影響腸道通透性。此外,各國不同的飲食習慣也反映在腸道疾病的發病率上。腸道高通透性病例往往發生在西方國家,那裏以富含脂肪和精制碳水化合物的飲食爲主。碳水化合物和脂質通過腸道菌群失調誘導細胞炎症,影響宿主胃腸道代謝和免疫穩態。長鏈脂肪酸是活細胞的重要組成部分,可以通過緊密連接的改變和組蛋白的乙酰化來影響腸道通透性。一些研究表明,果糖、葡萄糖和蔗糖與腸通透性增加和緊密連接功能障礙有關。
另一方面,一些碳水化合物,如低聚半乳糖,可以支持有益菌的生長,膳食纖維已被證明對腸道通透性具有積極影響。膳食纖維被酶和微生物消化,發酵産生短鏈脂肪酸,比如丁酸和丙酸,它們是保護腸道的關鍵因素。
此外,食品添加劑也與腸漏綜合征有關。最近的一篇綜述描述了食品添加劑通過幹擾緊密連接增加腸道通透性,促進免疫原性抗原進入機體的能力。另一方面,腸漏綜合征患者應多攝入膳食纖維,少攝入糖和脂肪。
有助于治療腸漏的成分
益生菌益生菌是攝入足夠數量對宿主健康具有有益作用的活性微生物。益生菌既存在于食物中,也作爲補充劑存在,最常見的食物是酸奶和開菲爾。服用益生菌的主要作用包括維持體內平衡和腸道完整性,調節腸道轉運,産生短鏈脂肪酸和維生素,消化膳食纖維以及中和外源性物質。益生菌還可以通過影響黏液、腸道上皮和腸道菌群,來幫助調節腸道通透性。
益生菌也具有抗炎作用,它們還可以增強黏膜屏障,降低腸道通透性,上調緊密連接蛋白。益生菌在結腸袋炎中的有利作用與黏膜屏障的穩態有關。
另一種可能的作用機制是産丁酸的微生物物種的加入。這些因素結合在一起,使腸道更完整,使益生菌成爲減少腸漏的絕佳療法。
多種乳酸杆菌對黏蛋白的表達和分泌具有影響。黏蛋白是覆蓋胃腸道上皮的黏液的主要蛋白質成分。這些糖基化大分子是由杯狀細胞合成的。它們位于細胞膜內或分泌到腸腔內形成黏膜層。在人類表達的18種黏蛋白樣糖蛋白中,黏蛋白MUC2是在小腸和大腸黏液中發現的主要糖蛋白。氨基和羧基末端的糖基化程度不同,但含有豐富的半胱氨酸殘基,可形成分子內和分子間的二硫鍵。這些聚糖基團賦予黏蛋白的蛋白水解抗性,而二硫鍵形成糖蛋白基質,是黏膜的骨架。
黏膜層保護上皮免受抗原和潛在有害分子的侵害,並作爲腸動力的潤滑劑。黏液是腸道細菌遇到的第一道屏障,病原體在感染過程中必須穿透黏液屏障到達上皮細胞。微生物已經發育出各種降解黏液的機制,比如黏蛋白二硫鍵還原、蛋白質水解活性和葡萄糖苷酶活性,以侵入黏液層或吸收來自黏液的營養物質。另一方面,結腸黏膜層在炎症區域更薄,允許更大的細菌黏附和浸潤。
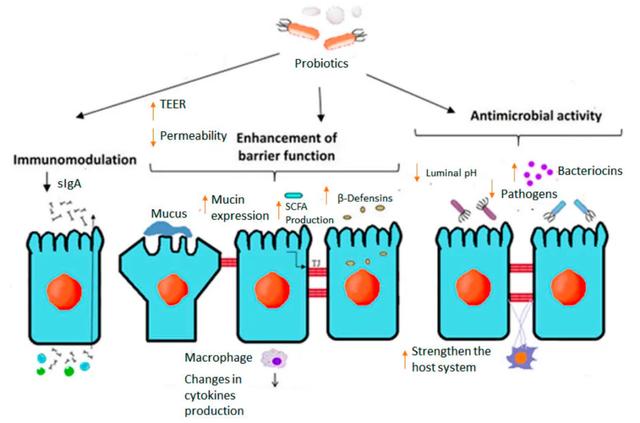
體外研究表明,多種乳酸杆菌,比如植物乳杆菌299v、鼠李糖乳杆菌GG和嗜酸乳杆菌DDS-1,可增加杯狀細胞表達和分泌黏蛋白,通過限制細菌穿過黏膜層的運動,來增強屏障功能和病原體清除。
益生菌對腸上皮的另一個積極作用是增加防禦素的表達和分泌。α-防禦素主要由小腸潘氏細胞表達,β-防禦素由整個腸道上皮細胞表達,它們具有對抗多種細菌、真菌和病毒的抗菌活性,阻止病原體到達腸上皮。就其本身而言,防禦素産生的減少與炎症性腸病的發生和細菌感染的易感性增加有關。細胞體外研究和人體研究表明,多種益生菌可以調節β-防禦素的表達和分泌。上皮細胞防禦素表達和黏液分泌的增加可以會阻止共生菌和病原菌的增殖,從而也有助于屏障的完整性。連續三周每天補充兩次益生菌的患者,糞便中β-防禦素hBD-2蛋白水平顯著升高,而接受安慰劑治療的患者糞便中hBD-2蛋白水平沒有變化。這些水平在停止益生菌治療後維持了9周,但程度較輕。
益生菌可增加黏膜固有層中産免疫球蛋白A (IgA)細胞的水平,促進黏膜管腔層分泌型IgA (sIgA)的分泌。這些抗體通過結合細菌及其抗原來限制上皮定植,有助于腸道內穩態。一些研究表明,某些微生物可以在感染後增加總IgA和病原特異性IgA的水平,而不增加益生菌特異性IgA的水平。給小鼠補充幹酪乳杆菌,可顯著增加産IgA細胞和産IL-6細胞的數量,從而刺激小鼠固有層內B細胞向IgA的類別轉換。此外,他們沒有發現針對幹酪乳杆菌的特異性抗體,這表明腸道免疫系統對這種有益細菌無反應。
不同的試驗測試了不同種類的益生菌對腸道通透性的有效性,包括鼠李糖乳杆菌GG、嗜酸乳杆菌、植物乳杆菌、嬰兒雙歧杆菌、乳雙歧杆菌BB-12和大腸杆菌Nissle 1917。它們參與調節腸上皮,修複腸道屏障,最終可能爲腸漏綜合征相關疾病提供潛在的健康益處。
維生素在大多數情況下,維生素A和D在調節胃腸道穩態中起著關鍵作用。在臨床試驗中,這些維生素影響黏膜屏障的組成,包括上皮完整性、免疫系統和腸道菌群。
研究表明,維生素A和D對腸道菌群組成的影響是間接的。在動物實驗中,這些維生素降低了微生物多樣性,增加了變形菌門細菌的數量,這對炎症性腸病患者具有潛在的致病性。在人體研究中,與維生素A缺乏的兒童相比,維生素A充足的兒童具有更多樣化的微生物群落。
在腸上皮中,體外研究表明維生素A和維生素D可改善緊密連接。維生素A和D對于維持腸上皮和腸道菌群的完整性以及在不同水平上調節免疫反應是必需的。這兩種維生素都能抑制T細胞産生IFN-γ,並在體外抑制Th17細胞。在體外模型中,這些維生素可以産生IL-10和FOXP3蛋白,這與免疫系統反應有關。維甲酸可以刺激腸細胞中抗菌肽的産生,比如Reg3β和Reg3γ。這些研究以及其它結果表明,維生素A和D在理論上的有利作用可能是由于調節黏膜屏障的不同元素。
膳食纖維和短鏈脂肪酸膳食纖維具有抗炎症和調節腸道屏障的作用。腸道菌群可發酵膳食纖維並産生短鏈脂肪酸,比如乙酸、丁酸和丙酸。特別是,有益的雙歧杆菌和乳酸杆菌與短鏈脂肪酸的産生以及對有害菌生長的免疫刺激和抑制作用有關。
短鏈脂肪酸是結腸上皮細胞的主要能量來源。丁酸是結腸細胞首選的最關鍵底物,可提供60-70%的能量需求。短鏈脂肪酸在代謝、免疫和腸道屏障功能中起著關鍵作用。例如,丁酸可以通過調節缺氧誘導因子-1和上皮緊密連接CLDN1來改善細胞旁通透性。此外,丁酸調節結腸黏液層的核心要素,以及人杯狀細胞樣LS174T細胞中杯狀細胞特異性黏蛋白MUC2的表達。
關于其抗炎特性,短鏈脂肪酸調節免疫細胞的趨化性,釋放活性氧和細胞因子。短鏈脂肪酸還可能通過控制免疫細胞向炎症部位的遷移並調節其活性,從而通過激活活性氧快速消除病原體,對炎症性疾病具有調節作用。上述過程有助于減少對宿主的損傷,這不僅可以使宿主存活,還有助于腸道細菌産生短鏈脂肪酸。
短鏈脂肪酸和膳食纖維的缺乏可通過增加腸道通透性損害腸上皮和黏膜屏障功能。在小鼠中,膳食纖維攝入不足和短鏈脂肪酸的産生不足可通過抑制嗜黏蛋白阿克曼氏菌(Akkermansia muciniphila)而損害腸道屏障的完整性。這種細菌在缺乏膳食纖維的情況下會利用黏液多糖作爲營養來源。這種改變可導致結腸黏液屏障受損,並導致腸道病原體鼠檸檬酸杆菌(Citrobacter rodentium)引起結腸炎的發生。
與健康志願者相比,那些診斷爲嚴重全身炎症反應綜合征的患者的短鏈脂肪酸水平發生了變化,乙酸、丙酸和丁酸的濃度顯著降低,pH值顯著升高。胃腸動力異常患者的有機酸和短鏈脂肪酸總濃度也都顯著降低。與健康志願者相比,作者還報告了炎症反應綜合征患者的專性厭氧細菌(擬杆菌、雙歧杆菌和腸杆菌)數量顯著降低,兼性厭氧微生物(腸球菌、葡萄球菌、假單胞菌和念珠菌)數量顯著增加。從長期來看,專性厭氧菌的減少可能會影響短鏈脂肪酸的濃度。
谷氨酰胺飲食中的谷氨酰胺在胃和十二指腸上部不會發生明顯的酸水解,因此可以到小腸中有效地吸收和代謝利用。除了吸收、分泌和消化的基本功能外,氨基酸對于滋養腸道健康至關重要,它是病原體、過敏原和毒素進入的屏障。
谷氨酰胺是一種至關重要的氨基酸,能夠調節緊密連接蛋白的表達,使腸細胞膜保持不可通透性。臨床前研究表明,添加谷氨酰胺可改善纖維化和腸道炎症。在T淋巴細胞、B淋巴細胞和上皮細胞中,谷氨酰胺可提高抗炎的IL-10水平,降低促炎IL-6和IL-8的産生。因爲IL-10對于維持腸黏膜穩態至關重要,這種氨基酸被認爲是先天和適應性免疫反應系統的調節器。
谷氨酰胺與益生菌聯合治療嚴重疾病患者的腸通透性具有有益效果。這種組合可以産生協同效應,增加乳酸杆菌的數量,減緩革蘭氏陰性菌的生長,改善腸道菌群結構,恢複結腸屏障的損傷。此外,它還能有效降低腸道黏膜的通透性和腸道內毒素水平,恢複腸屏障的機械損傷,從而減少腸道細菌的易位。
 精氨酸
精氨酸與谷氨酰胺不同,只有少數研究表明精氨酸對腸上皮完整性具有保護作用。
在腸梗阻模型中,精氨酸可降低腸道細胞旁通透性(400道爾頓分子)和大腸杆菌易位。同樣,L-精氨酸可適度地逆轉熒光黃試劑(457.25道爾頓)細胞旁通透性的增加和熱應激引起的跨膜電阻的降低。L-精氨酸對熱應激大鼠腸上皮屏障和IEC-6細胞系也具有保護作用。在IPEC-J2細胞中,精氨酸可改善缺氧誘導的細胞旁通透性,降低跨膜電阻,調節緊密連接蛋白ZO-1。
在非酒精性脂肪性肝炎齧齒動物的小腸中,精氨酸可調節緊密連接蛋白occludin和ZO-1並改善血漿細菌內毒素水平,保護動物免受非酒精性脂肪性肝炎的影響。精氨酸還可增強應激條件下低蛋白飲食禽類的腸道屏障功能。同樣,精氨酸對艾美球蟲攻擊或不攻擊的肉雞的整體生長、腸道完整性和形態均有有利影響。在小鼠腸道中,精氨酸可增加擬杆菌的數量,並增加mucin-2、mucin-4、TNF-α、IL-1β、IFN-γ、抗菌素和分泌型免疫球蛋白A的産生。
多酚類物質多酚類物質可通過NF-κB失活直接或間接參與腸道通透性,NF-κB途徑是細胞因子、白細胞介素和炎症的最重要調節者之一。此外,NF-κB激活與上皮屏障功能的損害有關。多酚類物質可通過抑制可降解的IκB蛋白酶體和幹擾IκB激酶磷酸化而使NF-κB失活。
另一個可能參與改善腸上皮功能的重要方面是抑制某些蛋白激酶,包括活化蛋白激酶、磷脂酰肌醇-3-激酶、酪氨酸激酶、絲裂原活化蛋白激酶、肌球蛋白輕鏈激酶、蛋白激酶C和單磷酸腺苷。表沒食子兒茶素沒食子酸酯(EGCG)、姜黃素和槲皮素等多酚類物質可通過抑制參與炎症性蛋白磷酸化的蛋白激酶C和肌球蛋白輕鏈激酶而降低腸道通透性。
最初,多酚類物質的有益作用歸因于它們清除活性氧的能力,即作爲抗氧化劑發揮作用。越來越多的證據表明,其益處與幹擾氧化還原信號通路的能力密切相關。人們認爲氧化應激可能參與腸道通透性增加的病因學,多酚類物質通常被建議用于治療這種疾病。研究表明,飲食中多酚類物質的攝入有助于恢複氧化還原穩態,提高抗氧化酶(SOD、CAT、GPx和GR)的活性。這些酶的表達受Nrf2的調控。Nrf2在細胞水平上被活性氧激活並易位到細胞核,在那裏調節編碼抗氧化酶的各種基因的轉錄,它是機體抗氧化防禦系統的主要調節因子,能夠增強細胞對氧化應激的抵抗。多酚類物質的抗氧化活性與激活Nrf2的能力有關,因此可以調節抗氧化酶活性。

多酚類物質可以增強緊密連接的完整性,增加黏液分泌,降低腸道屏障通透性,從而普遍改善腸道防禦機制。除了參與多種炎症信號通路外,多酚類物質還通過作用于腸上皮發揮有益作用,參與維持腸上皮穩態。最近的研究表明,富含多酚的飲食可以降低腸道屏障功能障礙的風險。槲皮素、沒食子兒茶素沒食子酸酯、兒茶素、表兒茶素、小檗堿、白藜蘆醇和姜黃素等多酚類物質已被深入研究,可提供對腸漏相關疾病的健康益處。
多酚類物質必須強調的一個關鍵方面是它們的生物利用度。據報道,在攝入多酚後,尿液和血漿樣本中僅檢測到總多酚的1-10%。
香草世界衛生組織估計,世界上80%以上的人口使用傳統醫學來滿足其初級保健需求,主要是使用植物提取物或其有效成分。香草可以作爲茶浸劑,茶煎劑,酒精提取物,非酒精提取物,酊劑,膠囊,藥膏和精油等形式使用。
各種香草含有有機酸、類黃酮、環烯醚萜苷、皂苷、綠原酸、烯醚萜、小檗堿、倍半萜烯和類倍半萜烯等植物化學物質,這些植物化學物質已被證明可治療肥胖、非酒精性脂肪性肝炎、潰瘍性結腸炎、克羅恩病、食物過敏、炎症性腸病和腸易激綜合征等疾病。
香草的作用機制很廣泛,包括調節腸道菌群和通透性,上調緊密連接claudin-1 mRNA和蛋白的表達,降低肝細胞胞外信號調節激酶的激活,抑制MLCK-MLC磷酸化信號通路,保護腸上皮細胞免受LPS損傷。最近的研究表明,在動物研究和臨床試驗中,香草可以緩解腸漏相關疾病。
蘑菇在過去的十年裏,蘑菇作爲功能性原料的使用越來越多。蘑菇是麥角甾醇、維生素D、酚類化合物、萜烯和萜類等生物活性化合物的重要來源。此外,蘑菇被認爲是益生元的可行來源,因爲它們含有不同的多糖,比如幾殼多糖、殼聚糖、半纖維素、木聚糖、甘露聚糖、半乳聚糖以及α-和β-葡聚糖。
從健康角度來看,蘑菇在免疫調節抗腫瘤活性、動脈粥樣硬化和肺炎球菌肺炎方面具有重要作用。在腸漏相關疾病中,蘑菇具有治療胰腺炎、非酒精性脂肪性肝病、結腸炎、肥胖和糖尿病的潛力。
蘑菇可通過刺激兒茶酚胺及其代謝物的産生和炎症反應,來調節腸道菌群。如前所述,蘑菇多糖也可以影響短鏈脂肪酸的産生,主要是乙酸、丙酸和丁酸。許多研究報道,蘑菇多糖有助于腸道擬杆菌門的增殖,而擬杆菌門細菌負責大多數乙酸和丙酸的産生。短鏈脂肪酸可以與許多受體相互作用,增強免疫信號和抗炎活性。短鏈脂肪酸可以作爲信號分子發揮作用,與遊離脂肪酸受體3和遊離脂肪酸受體2等G蛋白相關受體一起釋放調節緊密連接的GLP-1和GLP-2。
一些研究表明了蘑菇在維持腸上皮穩態和調節腸道菌群方面的健康益處。最近的研究也表明,蘑菇作爲益生元,可以促進腸道菌群的平衡和健康,對腸漏相關疾病發揮健康益處。

總結
人體胃腸道每天都與具有潛在毒性和感染性的物質接觸,胃腸道的抗原負荷非常大,它可以通過允許有益物質通過並阻斷有害物質通過來保護腸道完整性。在正常情況下,健康的腸道屏障可以阻止有毒元素進入血液;然而,腸壁完整性的破壞會有利于它們進入,可能引發疾病或炎症。
腸道菌群對維持腸上皮的完整性和穩態至關重要。腸道菌群組成的質和量的失衡或腸道生態失調會導致腸屏障功能障礙和腸漏綜合征。壓力、不健康飲食、過量飲酒、抗生素和藥物的使用等因素可損害腸道菌群的組成和腸道屏障功能的穩態,導致腸道通透性增加,發生腸漏。腸漏産生的腸道高通透性可使有害物質通過腸上皮的連接處進入血液,影響各器官和系統。因此,腸漏和腸屏障功能障礙與許多腸道疾病(比如炎症性腸病和腸易激綜合征)以及腸道外疾病(包括心髒病、肥胖、1型糖尿病和乳糜瀉)有關。考慮到腸道通透性與許多因素有關,我們可以方便地尋求一種良好的策略來避免或減少腸道通透性的增加。膳食營養素對屏障功能的影響對于開發腸漏相關疾病發病機制的新治療策略至關重要。
飲食是避免或減少腸漏發生,預防和治療腸漏相關疾病的最重要的方面。腸漏綜合征的治療應該包括飲食調整,避免脂肪、糖、食品添加劑和超加工食品的攝入,並適當地補充益生菌/益生元、精氨酸、谷氨酰胺、多酚類物質、維生素、膳食纖維、香草、可食用蘑菇等等。多項研究表明,這些成分會影響腸道免疫的調節、腸上皮屏障的調節、黏膜異常的改善和上皮細胞的生長,在腸漏及腸漏相關疾病的治療中發揮重要作用。
圖片來自網絡
參考資料:Aleman, R.S., et al. Leaky Gut and the Ingredients That Help Treat It: A Review. Molecules 2023, 28, 619.
