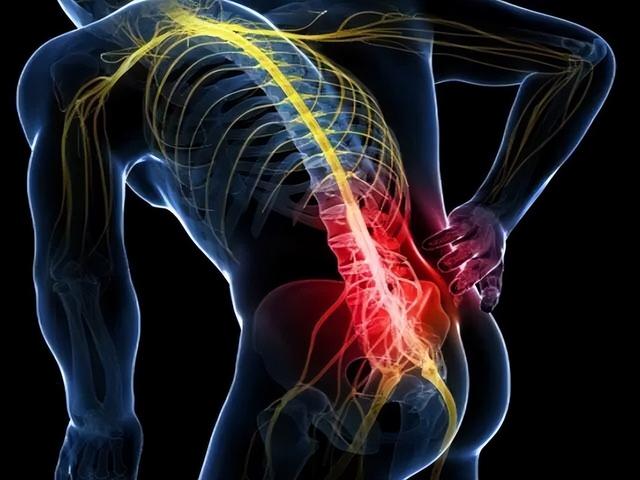
隨著人口老齡化的增加,脊柱退行性疾病患者的數量一直在上升。脊柱退行性疾病是由于脊柱結構退化引起的疾病的總稱,包括骨質疏松性椎體骨折(骨骼)、小關節骨關節炎(軟骨)、椎間盤退行性病變(椎間盤)、腰椎管狹窄(韌帶)和脊柱肌少症(肌肉)。此外,骨質疏松症、小關節骨關節炎、椎間盤退行性病變、腰椎管狹窄、脊柱肌少症往往並存,且發病率隨年齡增長而增加,對彼此的病理産生不利影響,形成惡性循環。
脊柱退行性疾病的風險因素包括衰老、繁重的勞動(機械應力)、創傷、遺傳、肥胖和代謝綜合征等。脊柱退行性疾病引起的疼痛和癱瘓已經成爲影響患者生活和工作的主要問題,給患者、家庭和社會造成了重大的經濟負擔。脊柱結構的漸進性退化不僅歸因于生物力學損傷或應激,還歸因于生物化學應激源,這些應激源會對脊柱結構中細胞和組織的正常活動産生不利影響。生物力學和生物化學因素之間複雜的相互作用,導致脊柱退行性病變的病理生理學。
隨著年齡的增長,會發生慢性低水平持續性組織炎症,這被稱爲“炎性衰老”,它已被報道與骨質疏松症、椎間盤退行性病變、骨關節炎和肌少症的發生有關。
腸道菌群參與一系列代謝、免疫、結構和神經功能,包括代謝穩態、免疫系統發育和成熟、抗感染和神經遞質的産生。腸道菌群及其代謝物在神經內分泌和免疫功能中發揮重要的調節作用,參與腸道內外各種器官的疾病過程,比如大腦、腎髒、肝髒、心髒和肌肉骨骼。腸道菌群還參與炎症性疾病的發生和發展,比如肥胖和代謝綜合征。腸道菌群的破壞已成爲誘導炎症細胞因子和有害細菌代謝物産生的潛在危險因素,可能參與包括脊柱退行性疾病在內的肌肉骨骼疾病的病理生理機制。
影響腸道菌群的因素與脊柱退行性疾病
健康的腸道菌群保持著一種動態的自我平衡狀態,由腸道菌群組成的豐富性和多樣性及其抵禦各種幹擾的穩定性和彈性所決定。腸道菌群的豐富性和多樣性可被環境因素(比如衰老)和生活方式因素(比如飲食、睡眠和運動)所改變。
衰老腸道菌群在與宿主共同進化的過程中,隨著年齡的變化,從嬰兒期到老年期會持續發生變化,機體衰老不可避免地伴隨著腸道菌群的變化。老年人的腸道菌群特征是多樣性和穩定性降低,産短鏈脂肪酸的基因表達減少,糖複合物降解能力降低,蛋白水解功能增強,表現爲變形菌門細菌富集,這個細菌門包含許多機會致病菌,而擬杆菌門和梭菌屬細菌的比例增加。
此外,衰老不僅影響腸道菌群的組成,還與腸腔和屏障功能的變化有關,包括腸保護性黏液層的收縮、腸緊密連接蛋白的喪失和腸上皮屏障的通透性增加。
近年來,出現了一種以細胞衰老爲中心的衰老觀。衰老的細胞會在各種哺乳動物物種(包括齧齒動物和靈長類動物)的組織和器官中表現出年齡依賴性的積累。存活的衰老細胞會分泌各種炎症細胞因子,促進慢性炎症和癌變。發生在老年人中的低水平慢性炎症,部分歸因于細胞衰老。隨著年齡的增長,衰老細胞負擔的增加會破壞組織結構和功能,並且正在成爲增加老年人疾病風險和死亡率的重要因素。骨質疏松症、肌肉減少症、椎間盤退行性病變和骨關節炎都是與細胞衰老相關的肌肉骨骼疾病。
衰老相關的氧化應激和炎症增加會促進衰老細胞的積累,應用抗氧化劑可以在體外和體內抑制細胞衰老。因此,中和氧化應激源可能會減弱或延緩衰老細胞的發生和積累。腸道菌群的各種代謝物具有很強的抗炎和抗氧化特性,可能有助于預防衰老相關的炎症和致瘤環境。相反,腸道菌群失調也會引起全身的慢性炎症應激,這可能會促進細胞衰老。腸道菌群失調也可能通過細胞衰老影響脊柱退行性疾病。因此,腸道菌群與人類衰老密切相關,腸道菌群的變化可以預測脊柱退行性疾病的發生和預後。
 生活方式因素(飲食、睡眠、運動)
生活方式因素(飲食、睡眠、運動)飲食、睡眠和運動是健康生活方式的三個關鍵組成部分,可以影響腸道菌群的組成和功能。
根據營養成分的差異,飲食可以顯著改變腸道菌群組成,這歸因于營養物質可以改變腸道菌群微環境,包括腸道菌群組成、代謝和宿主的免疫反應。
睡眠時間對腸道菌群的組成和功能也有顯著影響。睡眠時間短會促進腸道菌群異常,導致多樣性減少和抗炎腸道細菌減少,這可能會影響慢性炎症相關疾病。
運動可以對腸道菌群組成和代謝功能産生積極影響,並爲宿主提供健康益處。與久坐不動的人相比,運動員的腸道菌群多樣性高,且具有抗炎特性和較高的短鏈脂肪酸合成能力。
在年輕人和老年人的研究中,雙歧杆菌和普氏棲糞杆菌在有氧運動和阻力訓練後增加,糞便中短鏈脂肪酸丁酸的濃度增加。雙歧杆菌和普氏棲糞杆菌都參與短鏈脂肪酸的産生,可增強抗炎作用。
有規律的運動對老年人有益,尤其是那些超重的老年人,因爲它能保持腸道菌群組成和功能的穩定。運動在預防和治療脊柱退行性疾病方面的作用不僅僅限于典型的康複效果,比如改善肌肉功能、緩解疼痛和改善活動範圍,而且還包括改善腸道菌群組成和功能的協同效應,從而改善宿主的健康益處。
衰老、飲食變化、吸煙和飲酒、疾病、抗生素使用和病原體都可改變腸道菌群組成,導致菌群失調。腸道菌群失調可導致代謝和免疫調節網絡的失衡,從而導致炎症、組織破壞和疾病發生。
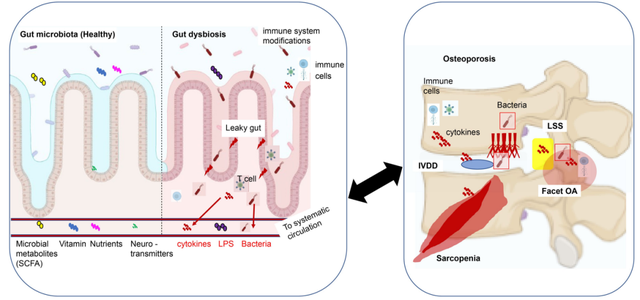
腸漏是腸道菌群失調的一個典型例子,其特征是腸壁對抗原的通透性改變,導致全身炎症和異常的免疫反應。當腸漏發生時,腸道菌群失去其保護能力,腸道屏障受損,細菌來源的化合物的擴散增強,代謝物和細胞因子的表達改變。這種失調的循環炎性細胞因子可能到達脊柱結構,包括骨骼、軟骨、椎間盤、韌帶和肌肉,從而破壞正常細胞信號和代謝活動。
在眼科,腸道菌群失調會引起慢性低度炎症,腸道通透性增加和IL-6、IL-1β、TNF-α和VEGF-A産生增加,最終導致脈絡膜新生血管的病理性血管生成加劇。類似的機制也可能存在于各種疾病的病理性血管生成中,包括脊柱退行性疾病。腸道菌群失調也可以改變腸壁通透性和生理代謝功能,破壞免疫、內分泌、血管和神經系統反應,最終導致免疫失調(過敏、自身免疫性疾病、炎症)、代謝疾病(糖尿病、代謝綜合征)、心血管疾病(冠狀動脈疾病)、神經發育障礙(自閉症)、神經退行性疾病(阿爾茨海默病)、癌症(胃癌、肺癌、結腸癌)甚至脊柱退行性疾病(骨質疏松症、小關節骨關節炎、椎間盤退行性病變、腰椎管狹窄)等疾病。
此外,無菌小鼠骨髓祖細胞的數量減少,表明腸道菌群會影響骨髓中的免疫細胞。人類脊柱有26塊椎骨,它們是免疫細胞的一大來源。腸道菌群失調可引起脊髓免疫細胞形成異常,導致全身炎症和背痛。總之,腸道菌群在衰老相關的慢性炎症相關疾病的病理發生中的作用和相關性不容忽視。
腸道菌群失調如何影響脊柱結構的健康?
在正常生理條件下,腸道菌群在宿主生理的各個方面發揮著基礎性作用,包括營養和代謝等功能,維持腸道屏障的完整性以阻止病原體入侵,並支持宿主的免疫反應。相反,這些功能的破壞可能導致炎症、疼痛和各種疾病的發生。
腸道菌群失調可通過以下三種機制影響脊柱結構的健康:
(1)營養,包括鈣、氨基酸和維生素等
腸道菌群可以調節鈣吸收,腸道菌群還參與維生素B和維生素K的合成,以及必需和非必需氨基酸、短鏈脂肪酸(乙酸、丙酸和丁酸)和神經遞質的産生。因此,腸道菌群通常被認爲是一種能夠影響遠端器官和系統功能的內分泌器官。
鈣的吸收以及維生素K和氨基酸的産生,對肌肉骨骼健康是必不可少的,這兩者都涉及腸道菌群。B族維生素的鎮痛、抗炎和神經保護作用已被廣泛記載。在B族維生素中,維生素B12被認爲對減輕背痛和神經痛有效。(2)雌激素、短鏈脂肪酸和系統性炎症相關的免疫調節
由于腸道菌群會分泌雌激素調節酶,腸道菌群的異常變化(比如多樣性降低)可能導致循環雌激素水平下降。絕經期雌激素缺乏是絕經後骨質疏松症的主要原因,絕經期雌激素缺乏會導致破骨細胞形成和骨吸收過多,導致骨質快速流失。雌激素水平降低會增加炎症和破骨細胞因子的産生,導致骨質疏松。失去雌激素免疫抑制作用的絕經後婦女,由于腸道菌群組成的變化引起的炎症狀態增加,可能會經曆更大的骨質流失。因此,腸道菌群與雌激素的相互作用會影響腸道菌群的組成和宿主組織對腸道菌群的反應,包括骨骼。短鏈脂肪酸是由腸道菌群發酵膳食纖維産生的,在調節腸道炎症和上皮屏障功能中起關鍵作用。此外,短鏈脂肪酸進入血液,會進一步促進全身炎症的調節。短鏈脂肪酸還影響代謝的各個方面,包括骨代謝、葡萄糖代謝、棕色脂肪組織激活、肝髒線粒體功能調節、全身能量穩態、食欲和睡眠調節。革蘭氏陰性菌的細胞壁成分脂多糖(LPS)是一種炎症性物質,作用于巨噬細胞,維持組織穩態並發揮促炎作用。LPS通過腸道和血液進入身體循環,可引起低水平的系統性炎症。LPS水平在慢性炎症性疾病中升高,比如肥胖、代謝綜合征、骨質疏松症、骨關節炎和椎間盤退行性病變。
(3)神經遞質和瘦素,它們會影響骨代謝,最終導致成骨細胞和破骨細胞之間的失衡
神經遞質,比如多巴胺、5-羟色胺、去甲腎上腺素、谷氨酸和γ-氨基丁酸,可由腸道菌群直接産生,也可由腸道菌群間接調節。至少50%的多巴胺在腸道中産生,並通過參與免疫反應在全身性炎症和慢性疼痛中具有調節功能。90%的5-羟色胺是在腸道中産生的,腸道來源的循環5-羟色胺會抑制骨形成並減少骨量。腸道菌群可以調節腸道中産生5-羟色胺的腸嗜鉻細胞。5-羟色胺還能調節與疼痛相關的生理功能。去甲腎上腺素也會引起疼痛和炎症。谷氨酸和γ-氨基丁酸在中樞神經系統中分別作爲主要的興奮性和抑制性神經代謝物,發揮各種重要的生理作用,包括調節疼痛。瘦素是一種脂肪細胞特異性的激素,可以調節骨形成,而腸道菌群積極調節全身瘦素水平,並參與骨代謝。因此,腸道細菌産生的一些分子是有益的,而另一些則是有害的,可以影響腸道內的內分泌細胞、腸道神經系統、腸道通透性和免疫系統。同時,腸道菌群組成和功能可能對脊柱退行性疾病相關的脊柱結構(比如骨骼、軟骨、椎間盤、韌帶和肌肉)的退行性病變和疼痛具有有益或有害的影響。
腸-脊柱軸
腸道菌群影響宿主代謝、免疫、內分泌環境和腸-腦-骨軸。它還通過多種潛在機制影響脊柱結構,包括骨骼、軟骨、椎間盤、韌帶和肌肉。
腸道菌群失調相關的炎症應激增加會促進脊柱肌肉骨骼細胞的衰老和脊柱結構中各種衰老細胞的積累。衰老細胞可能引起局部和全身性炎症,並促進以下脊柱退行性疾病的發生:骨質疏松症(衰老骨細胞和成骨細胞),骨關節炎(衰老軟骨細胞),椎間盤退行性病變(衰老髓核細胞)。
腸-骨軸:骨質疏松和骨質增生與骨代謝相關的脊柱退行性疾病包括骨質疏松性錐體骨折和骨質增生疾病,比如後縱韌帶骨化和彌漫性特發性骨骼增生。骨質疏松和骨質增生的發病機制涉及免疫炎症機制。骨骼是一個依賴于成骨細胞和破骨細胞之間的動態平衡來維持正常功能的器官。
近年來,腸道菌群對骨組織的影響已在無菌動物、使用抗生素清除腸道菌群的動物以及人類中得到了證實。此外,骨質疏松症的存在與腸道菌群組成和多樣性有關。
腸道菌群失調會導致骨質疏松症,也可能影響骨質增生疾病。後縱韌帶骨化和彌漫性特發性骨骼增生等骨質增生疾病與肥胖、2型糖尿病和代謝綜合征並發症密切相關,它們都表現出衰老相關的全身性低度炎症。此外,後縱韌帶骨化與瘦素和慢性炎症有關。如前所述,腸道菌群失調影響骨代謝,與低水平的慢性炎症相關疾病和神經遞質有關,這表明它不僅可能是骨質疏松症的病理因素,也可能是骨質增生疾病(比如後縱韌帶骨化)的病理因素。
因此,“腸-骨軸”表明腸道菌群通過營養吸收、炎症免疫和神經遞質與骨代謝相關,腸道菌群失調與骨質疏松症和骨質增生疾病之間存在強烈關聯。
 腸-關節軸:骨關節炎
腸-關節軸:骨關節炎“腸-關節軸”是基于腸道與關節之間可能的相互作用而建立的。
肥胖和代謝綜合征不僅是下肢負重關節發生骨關節炎的危險因素,也是非負重關節(腕關節和颞下颌關節)發生骨關節炎的危險因素。盡管機械和遺傳因素在骨關節炎的發生中起著重要作用,但越來越多的報道表明,低水平的全身性慢性炎症在骨關節炎的發生和進展中也起著重要作用。低水平的炎症與肥胖/代謝綜合征以及衰老、飲食和絕經後婦女的雌激素缺乏有關,所有這些都與骨關節炎和腸道菌群失調密切相關。
有研究表明,骨關節炎患者表現出明顯的腸道菌群失調,揭示了與骨關節炎相關的病原微生物的變化。此外,由于微生物存在于膝關節炎和髋關節炎中,腸道菌群失調導致的菌血症所引起的隱性或亞臨床細菌感染可能加重骨關節炎。
腸-椎間盤軸:椎間盤退行性病變椎間盤包括三個相互關聯的結構,即中央膠狀髓核、外纖維環和上下軟骨終板。椎間盤通常被認爲是人體最大的無血管化結構,在椎間盤退行性病變中可以檢測到血管侵入。
雖然椎間盤退行性疾病是多因素的,但慢性不受控制的低度炎症逐漸被發現與其病因有關。由于血液-椎間盤屏障的存在,使得椎間盤具有免疫特權,並保護它免受系統性感染,這也阻礙了免疫系統在椎間盤內的免疫監視。缺氧和缺乏免疫監視的椎間盤爲厭氧細菌在退行性病變的椎間盤中生長創造了理想的條件。這些生長在椎間盤中的細菌可以通過釋放炎症因子(比如IL-6、TNFα)來招募更多的炎症細胞(比如T細胞、B細胞、樹突狀細胞、巨噬細胞)。
因此,受損的椎間盤可以成爲逃避體液和細胞免疫的微生物生長和增殖以及有害微生物代謝物的傳播的理想場所。腸道菌群失調可能導致腸道細菌及其代謝物遷移到血液和椎間盤中,引發或加重椎間盤退行性病變。
2020年,印度的科研團隊評估24個腰椎間盤樣本,並報道健康椎間盤中的微生物組成與退行性病變的椎間盤和突出的椎間盤明顯不同。因此,“腸-椎間盤軸”的概念也正在出現,它可能在椎間盤退行性病變和腰痛中發揮重要作用。
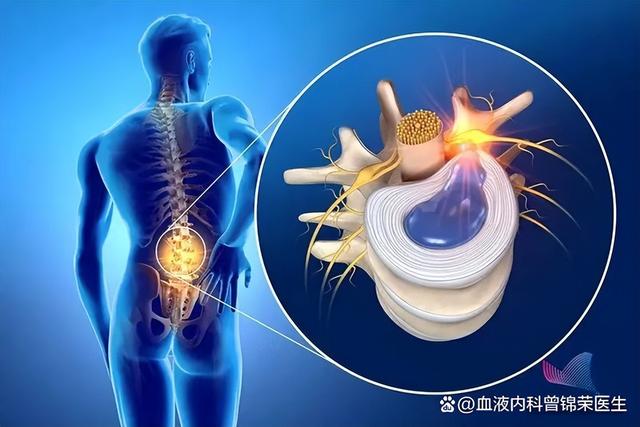 腸-韌帶軸:腰椎管狹窄
腸-韌帶軸:腰椎管狹窄除了小關節骨關節炎和椎間盤退行性病變外,黃腰韌帶增厚是腰椎管狹窄發病的主要原因,炎症相關的疤痕機制與腰韌帶增厚相關。
腰椎管狹窄與糖尿病、高血壓和代謝綜合征之間存在關聯,而這些疾病又都與腸道菌群失調密切相關,但沒有報道顯示腰椎管狹窄與腸道菌群菌群失調之間存在關聯。然而,椎間盤退行性病變和小關節骨關節炎作爲腰椎管狹窄相關的因素,都與腸道菌群有關系。此外,腰椎管狹窄患者的韌帶增厚中可觀察到炎症,表明腰椎管狹窄與腸道菌群之間也可能存在潛在的聯系,提示可能存在“腸-韌帶軸”。
腸-肌軸:脊柱肌少症肌少症被定義爲骨骼肌質量、力量和功能的進行性和系統性喪失。腸道菌群失調可通過炎症、免疫、蛋白質代謝、短鏈脂肪酸代謝和線粒體功能障礙影響肌肉量和功能,從而導致脊柱肌肉減少,最終影響宿主生理。
研究人員在肌肉減少症病例中觀察到腸道菌群多樣性和組成的顯著差異,並提出了“腸-肌軸”來解釋兩者之間的相互作用。由于脊柱肌少症(豎脊肌缺失)導致成人脊柱畸形的數量正在增加,其與腸道菌群的關系是一個有趣的研究課題。
腸道菌群對脊柱退行性疾病相關疼痛的影響脊柱退行性疾病的主要症狀包括腰痛以及上肢和下肢神經源性疼痛或麻木。由于腸道菌群參與了調節炎症和疼痛的短鏈脂肪酸、神經遞質和維生素的産生,因此它與脊柱退行性疾病相關疼痛密切相關是合理的。
腸道菌群會産生參與疼痛調節和鎮痛有關的神經遞質,包括多巴胺、5-羟色胺、去甲腎上腺素、谷氨酸和γ-氨基丁酸。此外,腸道菌群産生的B族維生素可以通過其抗炎和神經保護作用來發揮鎮痛作用。在腰痛、纖維肌痛、慢性疼痛、膝關節炎、手關節炎和周圍神經性疼痛患者中也發現了腸道菌群組成的異常,因此異常的腸道菌群組成可能與疼痛敏感性的個體差異有關。
然而,腸道菌群組成異常尚未證實與脊柱退行性疾病相關疼痛有關。了解腸道菌群與脊柱退行性疾病源性疼痛之間的相互作用可能有助于了解脊柱退行性疾病的發病機制。
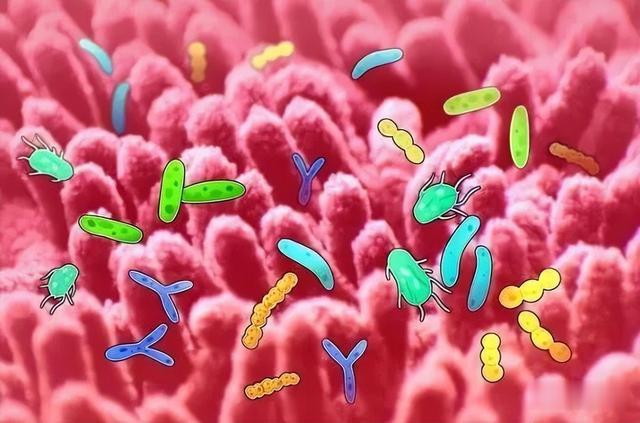
腸道菌群與脊柱肌肉骨骼疾病
骨骼:骨質疏松症與放線杆菌、布勞特氏菌、顫螺菌、擬杆菌和考拉杆菌正相關;關節:小關節骨關節炎與腸道菌群的關系無報道;椎間盤:許多已知的人類病原體,比如維羅尼假單胞菌、施氏假單胞菌、咽頰炎鏈球菌、蒼白普雷沃氏菌、雞鳥杆菌、考氏腸杆菌、譚氏普雷沃氏菌、嗜硝酸鹽單胞菌和非解乳糖鏈球菌,要麽在病變的椎間盤中豐度較高,要麽只存在于病變的椎間盤中;肌肉:肌少症與微生物多樣性降低以及毛螺菌、Fusicantenibacter、羅斯拜瑞氏菌、真杆菌和Lachnoclostridium的豐度下降有關;其它: 青少年特發性脊柱側彎者的普氏菌豐度增加;脊柱關節炎患者的産黑普雷沃氏菌、糞便普雷沃氏菌和普雷沃氏菌C561豐度增加,擬杆菌的豐度降低;牙龈卟啉單胞菌、肺炎克雷伯氏菌、産氣克雷伯氏菌和普通擬杆菌與強直性脊柱炎的病理發生相關。脊柱退行性疾病通常首先由椎間盤和小關節的退行性病變引起,也就是椎間盤退行性病變或小關節骨關節炎。結果,椎間體之間的穩定功能受損,導致椎間體和小關節周圍形成骨刺,黃韌帶增厚,導致腰椎管狹窄,包括腰椎滑脫。此外,脊柱肌少症和骨質疏松性椎體骨折可加速其病理。
由椎間盤退行性病變、小關節骨關節炎、腰椎管狹窄和骨質疏松性椎體骨折引起的脊柱退行性疾病相關疼痛會損害活動性,進一步加重腸道菌群失調、肌肉減少症和骨質疏松症。因此,骨質疏松症、椎間盤退行性病變、小關節骨關節炎、腰椎管狹窄和脊柱肌少症共存,不僅對脊柱退行性疾病有不利影響,而且腸道菌群失調也有不利影響,導致惡性循環。
調節腸道菌群可治療脊柱退行性疾病嗎?
由于脊柱退行性疾病在世界範圍內的流行,迫切需要有效的疾病改善治療策略來減輕症狀和減緩脊柱退行性疾病的進展。
腸道菌群通過腸-骨軸、腸-關節軸、腸-椎間盤軸、腸-韌帶軸和腸-肌軸等與遠端的脊柱結構相互作用。由于腸道菌群失調引起的菌血症和慢性低水平炎症會對脊柱結構産生不利影響,並導致脊柱退行性疾病的發病和進展,包括骨質疏松症、椎間盤退行性病變和骨關節炎。恢複腸道菌群失調也可能通過腸-骨軸、腸-關節軸、腸-椎間盤軸、腸-韌帶軸和腸-肌軸恢複生理調節,防止脊柱退行性疾病的發生和發展。
 生活方式(飲食、睡眠、運動)幹預腸道菌群可能改善脊柱退行性疾病
生活方式(飲食、睡眠、運動)幹預腸道菌群可能改善脊柱退行性疾病由于腸道菌群失調與脊柱退行性疾病和慢性炎症之間的關系,腸道菌群失調可能參與了脊柱退行性疾病的發生和發展。健康的生活方式(包括飲食、睡眠和運動等因素)可以改善腸道菌群組成,增加好細菌的數量,並可能改善腸道菌群失調。腸道菌群失調的改善也可能減輕炎症,抑制脊柱結構的退化,並通過短鏈脂肪酸或神經遞質來減輕疼痛。生活方式(飲食、睡眠、運動)與腸道菌群之間的相互作用有助于我們了解生活方式在預防和治療慢性炎症相關疾病中的作用,包括脊柱退行性疾病。
值得注意的是,包括益生元和益生菌在內的飲食幹預已顯示出通過調節腸道菌群來控制骨質疏松症和骨關節炎的良好效果。
益生元是不可消化的食物成分,比如膳食纖維和低聚糖,可以有益于健康的方式刺激消化道中有益菌的生長和/或活性,誘導短鏈脂肪酸合成,影響細胞生長和分化,激素産生和炎症調節,並對宿主産生有益作用。益生菌是攝入足夠數量,對宿主健康有益的活性微生物,通常是乳酸菌,它們調節上皮細胞、胃腸道平滑肌細胞中蛋白酶激活受體的表達,以調節胃腸道粘膜屏障功能和炎症。因此,它們通過促進上皮屏障功能和減少菌群失調,刺激抗菌物質和免疫球蛋白的産生,抑制細菌毒素的産生,從而促進宿主免疫反應和抗炎途徑,在維持健康的腸道菌群穩態中發揮重要作用。
據報道,益生元和益生菌都具有抗炎作用,促進鈣和維生素D的吸收,減少破骨細胞分化,保護骨骼和軟骨。它們也顯示出對骨質疏松症和骨關節炎的有益作用。
關于運動幹預,腸道菌群已被證明可以改善骨骼肌質量和功能,而運動可以影響腸道菌群的組成。此外,脊柱結構退行性病變的治療可以提高患者的運動水平,也會導致腸道菌群組成的改善。運動、腸道菌群和脊柱結構之間的這種良性循環關系可能有助于預防和治療脊柱退行性疾病。
睡眠障礙會促進腸道菌群失調,腸道細菌多樣性和抗炎腸道細菌減少,從而誘發全身性慢性炎症,這是慢性炎症相關性疾病(糖尿病和肥胖)的危險因素。慢性炎症與脊柱退行性疾病的發病和進展有關,因此,不能排除睡眠障礙和脊柱退行性疾病之間的聯系。相反,健康的睡眠可以促進脊柱退行性疾病的改善。
腸道菌群在藥物代謝中也具有重要作用,這可能影響藥物的療效。因此,通過改變生活方式來調節腸道菌群可能會提高鎮痛藥的療效,並有助于減少藥物用量。減少用藥是脊柱退行性疾病患者的一個關鍵問題,因爲多重用藥也是一個嚴重問題。在這方面,通過改善生活方式來腸道菌群也可能有效。

衆所周知,保持健康的生活方式是基于良好的營養、經常運動和充足的睡眠。然而,在脊柱外科領域,很少有研究調查健康生活方式與脊柱退行性疾病之間的關系。基于腸道菌群的生活方式幹預的治療效果,既是脊柱退行性疾病治療的新視角,也是對脊柱退行性疾病的有效治療。
糞菌移植糞菌移植是通過將健康供體的糞便細菌移植到患者的腸道中,幫助恢複患者的腸道菌群,從而達到治療疾病的效果。目前,糞菌移植在治療急性炎症(比如艱難梭菌感染)、慢性炎症(比如克羅恩病和潰瘍性結腸炎)方面非常有效。
糞菌移植在整個過程中保持了腸道菌群及其代謝物的完整性,從而最大限度地保留了腸道菌群的原有功能,顯著改善腸道菌群相關疾病,更快速有效地恢複腸道微環境穩態。疾病引起的生理破壞可以改變腸道菌群的組成和豐度,腸道菌群失調又會誘發或加劇疾病,而糞菌移植有望預防或緩解疾病狀況。
糞菌移植的潛在調節機制是重建正常的腸道環境和糾正腸道菌群的紊亂。它被認爲有可能恢複腸粘膜屏障,改善腸通透性,恢複腸道代謝物的失衡,並調節免疫反應。
糞菌移植已經在以下幾種腸道菌群失調相關疾病中得到了應用和驗證:
(1)胃腸道疾病:細菌性腸道感染(艱難梭菌感染)、炎症性腸病(克羅恩病和潰瘍性結腸炎)和腸易激綜合征;
(2)肝髒疾病:重度酒精性肝炎、原發性硬化性膽管炎、肝硬化;
(3)腦部疾病:自閉症譜系障礙、帕金森病、多發性硬化症、阿爾茨海默病、癫痫;
(4)代謝性疾病:糖尿病、肥胖、代謝綜合征、痛風;
(5)癌症:黑色素瘤、胃食道癌;
(6)皮膚病:脫發、特應性皮炎。
糞菌移植也可以有效改善骨質疏松症、銀屑病性關節炎和軸性關節炎。對于其它脊柱退行性疾病(骨關節炎、椎間盤退行性病變、腰椎管狹窄、脊柱肌少症),糞菌移植的作用尚未報道,腸道菌群失調可能會增加發生和進展的風險,進一步糾正腸道菌群組成和功能可能有助于預防、治療和症狀改善。
結論與展望
隨著社會老齡化,脊柱退行性疾病患者數量不斷增加,給患者及其家庭帶來了重大的社會經濟問題。脊柱退行性疾病是脊柱結構退行性疾病的總稱,包括骨質疏松症(骨骼)、小關節骨關節炎(關節)、椎間盤退行性病變(椎間盤)、腰椎管狹窄(韌帶)、脊柱肌少症(肌肉)等。
由于免疫、代謝和炎症等共同因素,腸道菌群與脊柱結構(骨骼、軟骨、椎間盤、韌帶和肌肉)之間的密切關系被稱爲腸-骨軸、腸-關節軸、腸-椎間盤軸、腸-韌帶軸和腸-肌軸。
腸道菌群失調引起的菌血症和慢性低水平炎症會對脊柱結構産生不利影響,並促進脊柱退行性疾病的發生和進展,包括骨質疏松症、腰椎管狹窄、椎間盤退行性病變、脊柱肌少症和脊柱退行性疾病相關疼痛。由于腸道菌群産生的神經遞質可以調節參與脊柱退行性疾病相關疼痛發生的外周神經系統神經元和疼痛感受器的興奮性,因此腸道菌群可能調節脊柱退行性疾病的發病機制和治療效果。腸道菌群和脊柱退行性疾病之間的密切聯系使研究人員提出了“腸-脊柱軸”的概念。
科學進步往往是由研究領域的明確劃分而推動,然而,要理解脊柱退行性疾病的複雜性和多面性,我們有必要整合不同學科的研究成果,比如脊柱解剖學、免疫學、微生物學、衰老等等。腸道菌群研究提供的觀點是這種跨學科整合的一個很好的例子,它可能不僅爲理解這些生物系統提供了一個新的框架,而且可能爲開發治療脊柱退行性疾病的有效療法提供許多有價值的見解。與炎症和腸道菌群失調相關的新生物標志物可能預測脊柱退行性疾病的發生並監測治療幹預的有效性。腸道菌群失調和菌血症導致的慢性炎症和不良免疫效應也可能導致脊柱退行性疾病術後感染。
脊柱退行性疾病的增加是老齡化社會的一個緊迫問題,預防很重要。預防醫學可分爲三級:一級預防(健康促進、抗衰老醫學、疾病預防)、二級預防(早發現、早治療、預防加重)和三級預防(康複、預防複發)。腸道菌群與脊柱相關退行性疾病的所有三級預防方面密切相關。
腸-脊柱軸視角可以爲脊柱退行性疾病的發病機制和治療提供新的見解。
圖片均來自網絡
參考資料:
Morimoto T, et al. (2023) Gut-spine axis: a possible correlation between gut microbiota and spinal degenerative diseases. Front Microbiol. 14: 1290858.
